
题目列表(包括答案和解析)

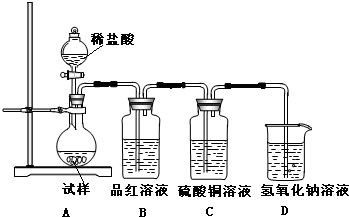 为探究亚硫酸钠的热稳定性,某研究性学习小组将无水亚硫酸钠隔绝空气加热,并利用受热后的固体试样和图所示的实验装置进行实验.请回答下列有关问题:
为探究亚硫酸钠的热稳定性,某研究性学习小组将无水亚硫酸钠隔绝空气加热,并利用受热后的固体试样和图所示的实验装置进行实验.请回答下列有关问题:
| ||
| ||

亚硝酸盐广泛存在于自然环境中,如蔬菜、肉类、豆类等都可以测出一定量的亚硝酸盐,一般情况下,当人体一次性摄取得300~500 mg亚硝酸钠时,就会引起中毒。某研究性学习小组用碘量法测定泡菜中亚硝酸盐的含量,反应方程式如下: 2NaNO2+2H2SO4+2KI==2NO+I2+K2SO4+Na2SO4+2H2O,2Na2S2O3+I2==Na2S4O6+2NaI。取l kg泡菜榨汁,将榨出的液体收集后,加入提取剂和氢氧化钠,使得到的泡菜汁中的亚硝酸盐都成为亚硝酸钠,在过滤后的滤液中加入氢氧化铝乳液,以除去色素,再次过滤后得到滤液,将该滤液稀释至1L,取25.00 mL菜汁与过量的稀硫酸和碘化钾溶液的混合液反应,再选用合适的指示剂,用较稀的硫代硫酸钠溶液进行滴定,共消耗0.050 mol·L![]() Na2S2O3溶液20.00 mL。请回答下列问题:
Na2S2O3溶液20.00 mL。请回答下列问题:
(1)该实验中可选用的指示剂是 。
(2)通过计算判断若某人一次食入0.125 kg这种泡菜,是否会引起中毒?
(3)有经验的厨师在做泡菜时往往加入适量的橙汁,以减轻亚硝酸盐的危害,主要是因为橙汁中含有丰富的维生素C,说明维生素C具有 性。
(12分)为探究亚硫酸钠的热稳定性,某研究性学习小组将无水亚硫酸钠隔绝空气加热,并利用受热后的固体试样和下图所示的实验装置进行实验。请回答下列有关问题: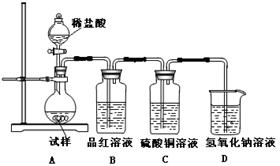
(1)查阅资料:无水亚硫酸钠隔绝空气受热到600℃才开始分解,且分解产物只有硫化钠和另外一种固体。如果加热温度低于600℃,向所得冷却后固体试样中缓缓滴加稀盐酸至足量,在滴加稀盐酸的整个过程中 的物质的量浓度变化趋势为 ;
的物质的量浓度变化趋势为 ;
(2)如果加热温度为700℃,向所得冷却后固体试样中缓缓滴加稀盐酸至足量,观察到烧瓶中出现淡黄色沉淀,且有大量气泡产生,则反应生成淡黄色沉淀的离子方程式为 ;此时在B、C两装置中可能观察到得现象为 。
(3)在(2)中滴加足量盐酸后,烧瓶内除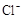 外,还存在另一种浓度较大的阴离子(X)。为检验该阴离子(X),先取固体试样溶于水配成溶液,为了加速固体试样的溶解,可采取措施。以下是检验阴离子(X)的两种实验方案,你认为合理的方案是 (填“甲”或“乙”),
外,还存在另一种浓度较大的阴离子(X)。为检验该阴离子(X),先取固体试样溶于水配成溶液,为了加速固体试样的溶解,可采取措施。以下是检验阴离子(X)的两种实验方案,你认为合理的方案是 (填“甲”或“乙”),
请说明另一方案不合理的原因 。方案甲:取少量试样溶液于试管中,先加稀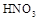 ,再加
,再加 溶液,有白色沉淀生成,证明该离子存在。
溶液,有白色沉淀生成,证明该离子存在。
方案乙:取少量试样溶液于试管中,先加稀HCl,再加 溶液,有白色沉淀生成,证明该离子存在。
溶液,有白色沉淀生成,证明该离子存在。
(4)写出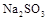 固体加热到600℃以上分解的化学方程式 。
固体加热到600℃以上分解的化学方程式 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com