
题目列表(包括答案和解析)
A.强酸强碱盐
B.强酸弱碱盐
C.强碱弱酸盐
D.上述三种盐均可能
|
已知一种c(H+)=1×10-3 mol/L的一元酸溶液和一种c(OH-)=1×10-3 mol/L的一元碱溶液等体积混合后溶液呈碱性,生成的盐是 | |
| [ ] | |
A. |
强酸强碱盐 |
B. |
强酸弱碱盐 |
C. |
强碱弱酸盐 |
D. |
上述三种盐均可能 |
已知25℃时部分弱电解质的电离平衡常数数据如表所示:
| 化学式 | CH3COOH | H2CO3 | HClO | |
| 电离平衡常数 | Ka=1.8×10-5 | Kal=4.3×10-7 | Ka2=5.6×10-11 | Ka=3.0×10-8 |

已知短周期主族元素X、Y、Z、W,原子序数依次增大且X和Y的原子序数之和等于Z的原子序数,X和Z可形成X2Z,X2Z2两种化合物,W是短周期主族元素中半径最大的元素.
(1)W在周期表中的位置:________.
(2)在一定条件下,容积为1 L密闭容器中加入1.2 mol X2和0.4 mol Y2,发生如下反应:3X2(g)+Y2(g)![]() 2YX3(g) ΔH反应各物质的量浓度随时间变化如下:
2YX3(g) ΔH反应各物质的量浓度随时间变化如下:

①此反应的平衡常数表达式为________(用化学式表示),K=________.
②若升高温度平衡常数K减小,则ΔH________0(填>,<).
(3)A1是四种元素中三种元素组成的电解质,溶液呈碱性,将0.1 mol·L-1的A1溶液稀释至原体积的10倍后溶液的pH=12,则A1的电子式为________.
(4)B1、B2是由四种元素三种形成的强电解质,且溶液呈酸性,相同浓度时B1溶液中水的电离程度小于B2溶液中水的电离程度,其原因是________.
(5)A2和B1反应生成B2,则0.2 mol/L A2和0.1 mol/L B1等体积混合后溶液中离子浓度大小关系为________.
已知短周期主族元素X、Y、Z、W,原子序数依次增大且X和Y的原子序数之和等于Z的原子序数,X和Z可形成X2Z,X2Z2两种化合物,W是短周期主族元素中半径最大的元素.
(1)W在周期表中的位置:________.
(2)在一定条件下,容积为1 L密闭容器中加入1.2 mol X2和0.4 mol Y2,发生如下反应:
3X2(g)+Y2(g)![]() 2YX3(g) ΔH
2YX3(g) ΔH
反应各物质的量浓度随时间变化如下:
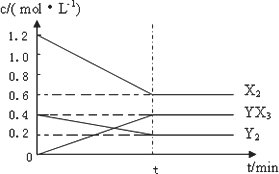
①计算该温度下此反应的平衡常数K=________.
②若升高温度平衡常数K减小,则ΔH________0(填“>”、“<”或“=”).
③改变下列条件,能使该平衡向正反应方向移动且平衡常数不变的是________(填字母).
a.增大压强
b.降低温度
c.使用催化剂
d.增大反应物的浓度
(3)常见液态化合物X2Z2的稀溶液易被催化分解,可使用的催化剂为________(填字母).
a.MnO2
b.FeCl3
c.Na2SO3
d.KMnO4
(4)A是四种元素中三种元素组成的电解质,溶液呈碱性,将常温下0.1 mol·L-1的A溶液稀释至原体积的10倍后溶液的pH=12,则A的电子式为________.
(5)以X2为燃料可制成燃料电池.已知:2X2(g)+Z2(g)=2X2Z(l) ΔH=?572 KJ·mol-1
该燃料电池释放228.8 KJ电能时,生成1 mol液态X2Z,该电池的能量转化率为________.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com