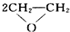[化学--选修2:化学与技术]
水是一种重要的自然资源,是人类赖以生存不可缺少的物质,水质优劣直接影响人体健康.请回答下列问题:
(1)某贫困山区,为了寻找合适的饮用水,对山上的泉水进行了分析化验,结果显示,水中主要含Ca
2+、Mg
2+、Cl
-和SO
.则该硬水的硬度属于
(填“暂时”或“永久”)硬度,若要除去Ca
2+、Mg
2+,可以往水中加入石灰和纯碱,试剂加入时先加
后加
.
(2)我国规定饮用水的硬度不能超过25度.硬度的表示方法是:将水中的Ca
2+和Mg
2+都看作Ca
2+,并将其折算成CaO的质量,通常把1L水中含有10mg CaO称为1度.某化学实验小组对本地区地下水的硬度进行检测.
═实验中涉及的部分反应:
M
2+(金属离子)+EBT(铬黑T)=MEBT
蓝色 酒红色
M
2+(金属离子)+Y
4-(EDTA)=MY
2-MEBT+Y
4-(EDTA)=MY
2-+EBT(铬黑T)
实验过程:
①取地下水样品25.00mL进行预处理.写出由Mg
2+引起的暂时硬度的水用加热方法处理时所发生反应的化学方程式:
;
②预处理的方法是向水样中加入浓盐酸,煮沸几分钟,煮沸的目的是
;
③将处理后的水样转移到250mL的锥形瓶中,加入氨水--氯化铵缓冲溶液调节pH为10,滴加几滴铬黑T溶液,用0.01000mol?L
-1的EDTA标准溶液进行滴定.滴定终点的颜色变化为
,滴定终点时共消耗EDTA溶液15.00mL,则该地下水的硬度为
.