
题目列表(包括答案和解析)
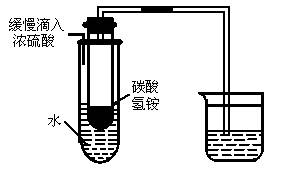
(1)烧杯中所盛的水溶液是_____________;发生反应的化学方程式为_____________________________________。
(2)小试管内的碳酸氢铵发生了什么变化?___________________,写出有关的化学方程式:__________________________。
(3)解释发生上述反应的原因:________________________________
(4)碳酸氢铵化肥应如何使用和保存?_________________________________________。
如图所示,当向大试管中缓缓加入浓硫酸时,烧杯中的水溶液会变浑浊,试回答:
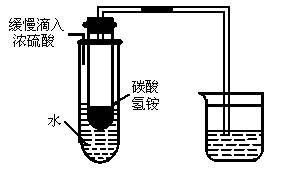
(1)烧杯中所盛的水溶液是_____________;发生反应的化学方程式为_____________________________________。
(2)小试管内的碳酸氢铵发生了什么变化?___________________,写出有关的化学方程式:__________________________。
(3)解释发生上述反应的原因:________________________________
(4)碳酸氢铵化肥应如何使用和保存?_________________________________________。
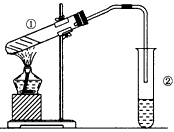
(12分)某学习小组为证明并观察铜与稀HNO3反应的产物是NO,设计了如下图所示的实验装置。请你根据他们的思路,回答有关的问题。
(一)实验仪器:大试管、玻璃导管、橡皮塞、烧杯、棉花、注射器。
(二)实验药品:铜丝、稀硝酸、碳酸钙颗粒、烧碱溶液。
(三)实验原理:
铜与稀硝酸反应的离子反应方程式 ① 。
(四)实验步骤:
1、按右图所示连接好装置,检验装置的 ② ;
2、向试管中加入一定量的固体药品(填化学式) ③ ,然后向试管中倒入过量的稀硝酸,并迅速塞紧带铜丝和导管的橡皮塞;
3、让试管中的反应进行一段时间后,用蘸有NaOH溶液的棉花团封住导管口;
4、将铜丝向下移动插入试管液体中,使之与稀硝酸反应;
5、把注射器的针孔插入试管口的橡皮塞中,缓慢向试管内推入空气。
(五)实验讨论:
1、实验步骤②的目的是(写出反应的离子方程式,结合文字说明)
④ ;
2、实验步骤⑤的目的是(写出反应的化学方程式,结合文字说明)
⑤ 。
(六)实验评价:
该装置的优点是(任写一个即可) ⑥ ;
有同学提出:增加右图所示装置,在步骤②完成后,当有明显现象再撤去该装置,并继续步骤③的“用蘸有NaOH溶液的棉花团封住导管口”。请评价他的做法 ⑦ 。
(12分)某学习小组为证明并观察铜与稀HNO3反应的产物是NO,设计了如下图所示的实验装置。请你根据他们的思路,回答有关的问题。

(一)实验仪器:大试管、玻璃导管、橡皮塞、烧杯、棉花、注射器。
(二)实验药品:铜丝、稀硝酸、碳酸钙颗粒、烧碱溶液。
(三)实验原理:
铜与稀硝酸反应的离子反应方程式 ① 。
(四)实验步骤:
1、按右图所示连接好装置,检验装置的 ② ;
2、向试管中加入一定量的固体药品(填化学式) ③ ,然后向试管中倒入过量的稀硝酸,并迅速塞紧带铜丝和导管的橡皮塞;
3、让试管中的反应进行一段时间后,用蘸有NaOH溶液的棉花团封住导管口;
4、将铜丝向下移动插入试管液体中,使之与稀硝酸反应;
5、把注射器的针孔插入试管口的橡皮塞中,缓慢向试管内推入空气。
(五)实验讨论:
1、实验步骤②的目的是(写出反应的离子方程式,结合文字说明)
④ ;
2、实验步骤⑤的目的是(写出反应的化学方程式,结合文字说明)
⑤ 。
(六)实验评价:
该装置的优点是(任写一个即可) ⑥ ;
有同学提出:增加右图所示装置,在步骤②完成后,当有明显现象再撤去该装置,并继续步骤③的“用蘸有NaOH溶液的棉花团封住导管口”。请评价他的做法 ⑦ 。

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com