
题目列表(包括答案和解析)
已知SO2 和H2S两种气体可以发生如下反应:2H2S + SO2 == 3S +2H2O
(1)常温下,向20L真空容器中通人a mol H2S 和 b mol SO2 (a、b都是正整数,且a≤5,b≤5)反应完成后,容器内气体可能达到的最大密度为 g/L
(2)在室温条件下,在一体积不变的的密闭容器中充入H2S和SO2气体,反应前压强为p,反应结束后压强为p/2,则反应前H2S和SO2的体积比是 或 。
已知SO2 和H2S两种气体可以发生如下反应:2H2S + SO2 == 3S +2H2O
(1)常温下,向20L真空容器中通人a mol H2S 和 b mol SO2 (a、b都是正整数,且a≤5,b≤5)反应完成后,容器内气体可能达到的最大密度为 g/L
(2)在室温条件下,在一体积不变的的密闭容器中充入H2S和SO2气体,反应前压强为p,反应结束后压强为p/2,则反应前H2S和SO2的体积比是 或 。
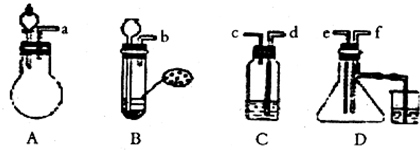
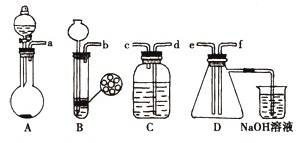 已知实验室制取H2S的实验原理为FeS(块状)+H2SO4═FeSO4+H2S↑.
已知实验室制取H2S的实验原理为FeS(块状)+H2SO4═FeSO4+H2S↑.| 压强/MPa 转化率/% 温度/℃ |
0.1 | 0.5 | 1 | 10 |
| 400 | 99.2 | 99.6 | 99.7 | 99.9 |
| 500 | 93.5 | 96.9 | 97.8 | 99.3 |
| 600 | 73.7 | 85.8 | 89.5 | 96.4 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com