
题目列表(包括答案和解析)
| 元素编号 | 元素性质或原子结构 |
| T | K层和M层上电子数之和等于L层上电数子 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| Z | 元素最高正价是+7价 |
 表示氢原子,
表示氢原子, 表示短周期的相邻的三种元素原子.小黑点表示没有形成共价键的最外层电子,短线表示共价键
表示短周期的相邻的三种元素原子.小黑点表示没有形成共价键的最外层电子,短线表示共价键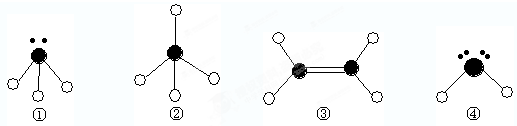
现有部分短周期元素的性质或原子结构如下表:
| 元素编号 | 元素性质或原子结构 |
| T | M层上的电子数是原子核外电子层数的2倍 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下单质为双原子分子,其氢化物的水溶液呈碱性 |
| Z | 元素最高正价是+7价 |
完成下列问题:
(1)元素T在周期表中位于第______周期第______族.
(2)元素X的一种同位素可测定文物年代,其原子核内有8个中子,这种同位素的符号是________.
(3)元素Y与氢元素形成一种分子YH3,写出该粒子的电子式____________.
(4)元素Z与元素T相比,非金属性较强的是________(用元素符号表示),下列表述中能证明这一结果的是________________________________.
a.常温下Z的单质和T的单质状态不同
b.Z的氢化物比T的氢化物稳定
c.一定条件下Z和T的单质都能与NaOH溶液反应
(5)T、X、Z三种元素的最高价氧化物的水化物的酸性由强到弱的顺序是________________(用化学式表示).
(10分)下列分子结构图中的 表示氢原子,
表示氢原子, 表示短周期的相邻的三种元素原子。小黑点表示没有形成共价键的最外层电子,短线表示共价键。
表示短周期的相邻的三种元素原子。小黑点表示没有形成共价键的最外层电子,短线表示共价键。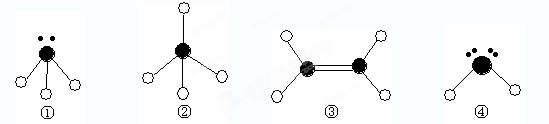
(1)以上分子中,中心原子采用sp2杂化的是 (填化学式);
(2)在③的分子中有 个σ键。在③与溴的四氯化碳溶液反应中,断裂的是③分子中的 键(填“σ”或“π”),形成的是 键(填“σ”或“π”)。
(3)4种分子中,属于极性分子的是 (填序号,下同)。键角由大到小的顺序是 ,能结合质子(即H+)形成稳定离子的是 ,形成 键(按电子对提供方式分类)。
(4)已知液态①和④相似,也可发生微弱的电离,电离出含有相同电子数的微粒,则①的电离方程式为: ;
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com