
题目列表(包括答案和解析)
+ 4 |
+ 4 |
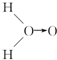 (式中O→O表示配位键,在化学反应中O→O键遇到还原剂时易断裂)
(式中O→O表示配位键,在化学反应中O→O键遇到还原剂时易断裂)

(1)γ-Fe的晶体结构是图3-22中的“a”还是“b”?_____________________?
(2)α-Fe或σ-Fe的空间利用率是多少?_____________________
(3)从晶体结构的空间利用率分析,在给纯铁加热的过程中,在
(4)在纯铁中掺入半径较小的非金属原子,如硼、碳、氮、氢等可形成特殊结构。具有这种结构的物质同时存在金属键和共价键,原子间结合得特别牢固,请推测它们具有的优异性能。_______________________________________________________________
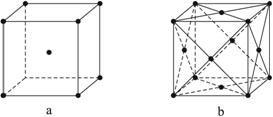
图3-22
下列说法不正确的是( )。
A.NH4NO3、NaOH中既有离子键,又有极性共价键,其中NH4NO3中还有配位键
B.水的沸点是100℃,硫化氢的分子结构跟水相似,但它的沸点却很低,是-60.7℃,引起这种差异的主要原因是水分子间有氢键
C.范德华力与氢键可同时存在于分子之间
D.氢键比范德华力强,且氢键是一种特殊的化学键
下列说法不正确的是( )。
| A.NH4NO3、NaOH中既有离子键,又有极性共价键,其中NH4NO3中还有配位键 |
| B.水的沸点是100℃,硫化氢的分子结构跟水相似,但它的沸点却很低,是-60.7℃,引起这种差异的主要原因是水分子间有氢键 |
| C.范德华力与氢键可同时存在于分子之间 |
| D.氢键比范德华力强,且氢键是一种特殊的化学键 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com