
题目列表(包括答案和解析)
元素
R的化合价以偶数递增, R的一种氧化物中含氧的质量分数为60%, R原子具有的电子层数是[ ]
A.1层 B.2层 C.3层 D.4层
某元素的一种同位素R具有微弱放射性,其原子核内中子数比质子数多43,由它组成的固体单质A,在一定条件下密度为6.88 g/m3,用X射线研究其固体表明,在边长为1.00×10-7 cm的立方体中含有20个原子。
R在化学反应中常表现为+2、+4价,在溶液中R2+稳定,而R4+有强氧化性,可将NO氧化为HNO3。回答:
(1)R的摩尔质量为__________。
(2)R处于周期表第__________周期__________族。
(3)将含R4+的溶液加入到Fe(NO3)2溶液中,反应的离子方程式为________________。
某元素的一种同位素的原子R,其质量数为A,![]() 核外电子数为x,则W
g
核外电子数为x,则W
g ![]() 中所含中子的物质的量为
中所含中子的物质的量为
[ ]
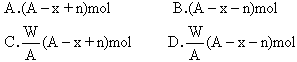





(1)n和m的值。
(2)R的相对原子质量。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com