
题目列表(包括答案和解析)
①CH3COOH(l)+2O2(g)![]() 2CO2(g)+2H2O(l) ΔH(298 K)=-870.3 kJ·mol-1
2CO2(g)+2H2O(l) ΔH(298 K)=-870.3 kJ·mol-1
②C(s)+O2(g) ![]() CO2(g) ΔH(298 K)=-393.5 kJ·mol-1
CO2(g) ΔH(298 K)=-393.5 kJ·mol-1
③H2(g)+![]() O 2(g)
O 2(g) ![]() H2O(l) ΔH=-285.5 kJ·mol-1
H2O(l) ΔH=-285.5 kJ·mol-1
试求:④![]() CH3COOH(l)的ΔH。
CH3COOH(l)的ΔH。
①CH3COOH(l)+2O2(g)![]() 2CO2(g)+2H2O(l) ΔH(298 K)=-870.3 kJ·mol-1?
2CO2(g)+2H2O(l) ΔH(298 K)=-870.3 kJ·mol-1?
②C(s)+O2(g)![]() CO2(g) ΔH(298 K)=-393.5 kJ·mol-1?
CO2(g) ΔH(298 K)=-393.5 kJ·mol-1?
③H2(g)+![]() O2(g)
O2(g)![]() H2O(l) ΔH=-285.8 kJ·mol-1
H2O(l) ΔH=-285.8 kJ·mol-1
试求:④![]() CH3COOH(l)的ΔH。?
CH3COOH(l)的ΔH。?
若已知以下反应和衍生关系:
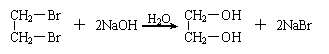
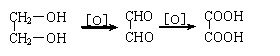
现在实验室用淀粉以及必要的无机原料,制备乙二酸乙二酯(环)(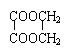 ),请用化学方程式表示(注明条件、主要物质名称和反应类型)。
),请用化学方程式表示(注明条件、主要物质名称和反应类型)。
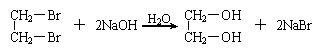
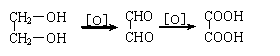
现在实验室用淀粉以及必要的无机原料,制备乙二酸乙二酯(环)(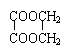 ),请用化学方程式表示(注明条件、主要物质名称和反应类型)。
),请用化学方程式表示(注明条件、主要物质名称和反应类型)。
 FeO(s)+CO(g);△H=Q1的平衡常数为 K1,反应②Fe(s)+H2O(g)
FeO(s)+CO(g);△H=Q1的平衡常数为 K1,反应②Fe(s)+H2O(g)  FeO(s)+H2(g);△H=Q2的平衡常数为K2,在不同温度下,K1、K2的值如下:
FeO(s)+H2(g);△H=Q2的平衡常数为K2,在不同温度下,K1、K2的值如下:| T/K | K1 | K2 |
| 973 | 1.47 | 2.38 |
| 1 173 | 2.15 | 1.67 |
 CO(g)+H2O(g);△H=Q3平衡常数为K3.
CO(g)+H2O(g);△H=Q3平衡常数为K3.| k1 |
| k2 |
| k1 |
| k2 |


湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com