ЕдО»ЖҪәвТІКЗТ»ЦЦПа¶ФЖҪәвЧҙМ¬Ј¬ҙжФЪЧЕЖҪәвТЖ¶ҜЈ¬ЛьН¬ИЬТәөДpHЦөЎўіБөнөД·ҙУҰЎўСх»Ҝ»№Фӯ·ҙУҰөИУРГЬЗР№ШПөЈ¬ТІҫНКЗЛөЈ¬ФЪИЬТәЦРРОіЙЕдО»ОпКұЈ¬іЈіЈіцПЦСХЙ«өДұд»ҜЎўИЬҪв¶ИөДұд»ҜЎўPHЦөөДёДұдөИПЦПуЈ®Br
-УлCu
2+·ҙУҰЙъіЙЕдО»»ҜәПОпЈ¬ҫНҙжФЪЕдО»ЖҪәвЈ® Cu
2++2Br
-?Cu Br
2Cu
2++4Br
-?[Cu Br
4]
2-ТСЦӘЈәCu
2+ФЪЛ®ИЬТәЦРПФА¶Й«Ј¬[Cu Br
4]
2-ФЪЛ®ИЬТәЦРПФ»ЖЙ«Ј¬А¶Й«Ул»ЖЙ«ІўҙжКұПФВМЙ«Ј¬[Cu Br
4]
2-ЕЁ¶ИФҪҙуЈ¬СХЙ«ФҪЙоЈ®Н¬КұЈ¬ОВ¶ИҝЙДЬ¶Ф[Cu Br
4]
2-өДОИ¶ЁРФУРУ°ПмЈ®
Ді»ҜС§МҪҫҝРЎЧйөДН¬С§ОӘБЛМҪҫҝОВ¶ИЎўЕЁ¶И¶ФBr
-УлCu
2+өДЕдО»ЖҪәвөДУ°ПмЈ¬УЪКЗЧцБЛПВБРөДјЩЙиУлІВПлЈЁМоРҙҝХИұөДјЩЙиЈ©Јә
[јЩЙиУлІВПл]
1ЎўФцҙуЕдО»АлЧУЈЁBr
-Ј©өДЕЁ¶ИЈ¬ЖҪәвПтХэ·ҙУҰ·ҪПтТЖ¶ҜЈ¬ЙъіЙЕдәПОпөДЕЁ¶ИФцҙуЈ¬ИЬТәСХЙ«јУЙоЈ»
2Ўў
ФцҙуCu2+өДЕЁ¶ИЈ¬ЖҪәвПтХэ·ҙУҰ·ҪПтТЖ¶ҜЈ¬ЙъіЙЕдәПОпөДЕЁ¶ИФцҙуЈ¬ИЬТәСХЙ«јУЙоЈ»
ФцҙуCu2+өДЕЁ¶ИЈ¬ЖҪәвПтХэ·ҙУҰ·ҪПтТЖ¶ҜЈ¬ЙъіЙЕдәПОпөДЕЁ¶ИФцҙуЈ¬ИЬТәСХЙ«јУЙоЈ»
Ј®
3ЎўОВ¶Иұд»ҜҝЙДЬУ°ПмЕдәПОпөДОИ¶ЁРФЈ¬ҙЩҪшЕдәПОпөДРОіЙЈ¬ЖҪәвПтХэ·ҙУҰ·ҪПтТЖ¶ҜЈ®
4ЎўОВ¶Иұд»ҜТІҝЙДЬК№»ҜС§ЖҪәвПтЧуТЖ¶ҜЈ¬ТЦЦЖЕдәПОпөДРОіЙЈ®
[КөСйЧјұё]
ЈЁ1Ј©CuSO
4ИЬТәөДЧјұёЈә·ЦұрИЎ3·Э8gОЮЛ®CuSO
4№ММеЈ¬ёчјУИлЛ®ПЎКНөҪ100mlЎў50mlЎў25mlЈЁөЪИэЦЦИЬТәТСұҘәНЈ©Ј»
ЈЁ2Ј©NaBrИЬТәөДЧјұёЈә·ЦұрИЎ2.06gЎў4.12gЎў4.12gNaBrҫ§МеЈ¬ёчјУИлЛ®ПЎКНөҪ50mlЎў50mlЎў25mlЈ®
ОКМв1ЈәҙЦВФЕдЦЖЙПКцИЬТәРиТӘУГөҪөДТЗЖчУРЈә
ЈЁНРЕМЈ©МмЖҪЎўЙХұӯЎўІЈБ§°фЎўБҝНІ
ЈЁНРЕМЈ©МмЖҪЎўЙХұӯЎўІЈБ§°фЎўБҝНІ
Ј»
ұн1ЎўІ»Н¬ЕЁ¶ИөДBr
-ИЬТәУлДіТ»ЕЁ¶ИөДCu
2+ИЬТә·ҙУҰ
| ұаәЕ |
5mlCu2+ИЬТәЈЁmol?L-1Ј© |
10ml Br-ИЬТәЈЁmol?L-1Ј© |
ПЦПу |
| ўЩ |
өЪТ»·ЭCuSO4ИЬТә |
a |
ИЬТәУЙА¶Й«ұдОӘА¶ВМЙ« |
| ўЪ |
өЪТ»·ЭCuSO4ИЬТә |
b |
ИЬТәУЙА¶Й«ұдОӘІЭВМЙ« |
| ўЫ |
өЪТ»·ЭCuSO4ИЬТә |
c |
ИЬТәУЙА¶Й«ұдОӘББВМЙ« |
ұн2ЎўІ»Н¬ЕЁ¶ИөДCu
2+ИЬТәУлДіТ»ЕЁ¶ИөДBr
-ИЬТә·ҙУҰ
| ұаәЕ |
5mlCu2+ИЬТәЈЁmol?L-1Ј© |
10ml Br-ИЬТәЈЁmol?L-1Ј© |
ПЦПу |
| ўЩ |
d |
өЪТ»·ЭNaBrИЬТә |
ИЬТәУЙА¶Й«ұдОӘА¶ВМЙ« |
| ўЪ |
e |
өЪТ»·ЭNaBrИЬТә |
ИЬТәУЙА¶Й«ұдОӘІЭВМЙ« |
| ўЫ |
f |
өЪТ»·ЭNaBrИЬТә |
ИЬТәУЙА¶Й«ұдОӘББВМЙ« |
ұн3ЎўІ»Н¬ОВ¶И¶ФЕдәПОпРОіЙөДУ°Пм
| ұаәЕ |
5mlCu2+ИЬТәЈЁmol?L-1Ј© |
10ml Br-ИЬТәЈЁmol?L-1Ј© |
ОВ¶И |
ПЦПу |
| ўЩ |
өЪТ»·ЭCuSO4ИЬТә |
өЪТ»·ЭNaBrИЬТә |
25Ўж |
ИЬТәУЙА¶Й«ұдОӘА¶ВМЙ« |
| ўЪ |
өЪТ»·ЭCuSO4ИЬТә |
өЪТ»·ЭNaBrИЬТә |
60Ўж |
ИЬТәУЙА¶Й«ұдОӘІЭВМЙ« |
| ўЫ |
өЪТ»·ЭCuSO4ИЬТә |
өЪТ»·ЭNaBrИЬТә |
75Ўж |
ИЬТәУЙА¶Й«ұдОӘББВМЙ« |
ОКМв2ЈәЙПұнЦРb=
0.8
0.8
mol/LЈ¬e=
1.0
1.0
mol/LЈ»
ОКМв3ЈәНЁ№эұн3өГіцөДҪбВЫКЗ
ОВ¶ИЙэёЯУ°ПмЕдәПОпөДОИ¶ЁРФЈ¬ҙЩҪшЕдәПОпөДРОіЙЈ¬ЖҪәвПтХэ·ҙУҰ·ҪПтТЖ¶ҜЈ®
ОВ¶ИЙэёЯУ°ПмЕдәПОпөДОИ¶ЁРФЈ¬ҙЩҪшЕдәПОпөДРОіЙЈ¬ЖҪәвПтХэ·ҙУҰ·ҪПтТЖ¶ҜЈ®
Ј»
ОКМв4ЈәЙПКц·ҙУҰёщҫЭөДФӯАнКЗ
АХЙіМШБРФӯАнЈЁ»т»ҜС§ЖҪәвТЖ¶ҜФӯАнЈ©Ј®
АХЙіМШБРФӯАнЈЁ»т»ҜС§ЖҪәвТЖ¶ҜФӯАнЈ©Ј®
Ј®

 COЈЁgЈ©+3H2ЈЁgЈ©ЎчH=+206.1kJ?mol-1Ј®
COЈЁgЈ©+3H2ЈЁgЈ©ЎчH=+206.1kJ?mol-1Ј®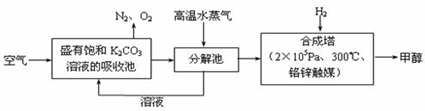
 №эСх»ҜЗвКЗЦШТӘөДСх»ҜјБәН»№ФӯјБЈ¬іЈУГУЪПы¶ҫЎўЙұҫъЎўЖҜ°ЧөИЈ®Ді»ҜС§РЛИӨРЎЧйН¬С§О§ИЖЧЕ№эСх»ҜЗвҝӘХ№БЛөчІйСРҫҝУлКөСйЈ®
№эСх»ҜЗвКЗЦШТӘөДСх»ҜјБәН»№ФӯјБЈ¬іЈУГУЪПы¶ҫЎўЙұҫъЎўЖҜ°ЧөИЈ®Ді»ҜС§РЛИӨРЎЧйН¬С§О§ИЖЧЕ№эСх»ҜЗвҝӘХ№БЛөчІйСРҫҝУлКөСйЈ®