
题目列表(包括答案和解析)
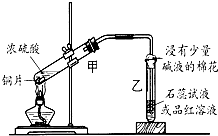 浓硫酸与铜的反应用了如图所示的装置,请回答下列问题.
浓硫酸与铜的反应用了如图所示的装置,请回答下列问题.
| ||
| ||
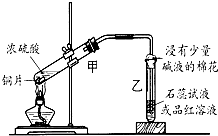 浓硫酸与铜的反应用了如图所示的装置,请回答下列问题.
浓硫酸与铜的反应用了如图所示的装置,请回答下列问题.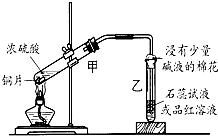
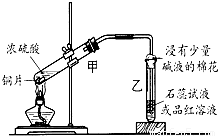
某同学用下图所示的装置来验证浓硫酸与铜是否发生反应并探讨反应所产生气体的性质.请回答下列问题:

(1)通过试管乙中发生的________现象说明了铜和浓硫酸发生了化学反应,并且该现象还能说明产生的气体具有________.
(2)试管甲中发生反应的化学方程式________.
(3)试管乙口部浸有碱液的棉花的作用是________.
(4)SO2的排放是造成酸雨的主要因素,某同学通过实验探究,得出酸雨pH随时间的增加而减小的结论.其原因是________(用化学方程式表示).
(5)
为进一步研究酸雨的成分,该同学取某一时段的这种雨水V L,加入0.5 mol·L-1的Ba(OH)2溶液至不再产生沉淀时,恰好消耗40.00 mL Ba(OH)2溶液.请计算:①
该V L雨水中共溶解的SO2体积是________mL(标准状况).②
若在上述实验中生成沉淀物的质量为4.50 g,该沉淀物的成分是:________.湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com