
题目列表(包括答案和解析)
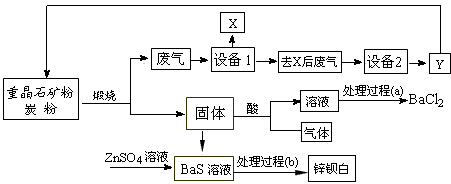
工业上用重晶石(主要成分BaSO4)为原料制备BaCl2和锌钡白,生产过程中会产生大量废气(主要成分为CO2、CO及少量SO2和硫蒸气等),为防止污染空气并提高原料利用率,生产中采用下述工艺流程:

请根据上述流程回答下列问题:
(1) 假设煅烧时还原产物只有BaS,则反应的化学方程式为______________________。
(2) 设备2中所用的洗涤剂是碱液,则Y的化学式为________。
(3) 溶解固体所用的酸为________(填化学式),生成的气体用过量NaOH溶液吸收,其反应的离子方程式为_______________________________________________。
(4) 处理过程(b)的具体步骤为____________________。
(5) 锌钡白的成分是____________(填化学式)。
工业上用硫铁矿为主要原料抽取硫酸,主要设备有沸腾米,接触室和吸引塔。
(1)硫铁矿在进入沸腾炉前需要粉碎,其目的是 。
(2)为了充分利用反应放出的热量,接触室中应安装 (填设备名称);吸引塔中填充许多瓷管,其作用是 。
(3)吸收塔排放的尾气中含有少量的SO ,防止污染大气、充分利用原料,在排放前必须进行尾气处理并设法进行综合利用。
,防止污染大气、充分利用原料,在排放前必须进行尾气处理并设法进行综合利用。
传统的方法是:尾气中的SO 通常用足量氨水吸收,然后再用稀硫酸处理,写出上述过程中的化学反应方程式:
,其优点是
。
通常用足量氨水吸收,然后再用稀硫酸处理,写出上述过程中的化学反应方程式:
,其优点是
。
创新方法是:将尾气中的SO 用Na
用Na SO
SO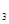 溶液吸收,然后再加热所得溶液,写出上述过程中的化学反应方程式:
,创新方法与传统方法相比,其优点是 。
溶液吸收,然后再加热所得溶液,写出上述过程中的化学反应方程式:
,创新方法与传统方法相比,其优点是 。
(4)在硫酸的工业制法中,下列生产操作及说法生产操作的主要原因二者都正确的是 (填序号)
A.从沸腾炉出来的炉气需净化,因为炉气中的SO 与杂质反应
与杂质反应
B.硫酸生产中常采用高压条件,目的是提高SO 的转化率
的转化率
C.SO 被氧化为SO
被氧化为SO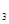 时需要使用催化剂,这样可以提高SO
时需要使用催化剂,这样可以提高SO 的转化率
的转化率
D.SO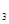 用98.3%浓硫酸吸收,目的是防止形成酸雾,有利于SO
用98.3%浓硫酸吸收,目的是防止形成酸雾,有利于SO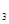 吸收完全
吸收完全
(5)某硫酸厂若要生产8吨98%的浓硫酸至少需要标准状况下的空气
m ( O
( O 空气中的体积分数按20%计算)。
空气中的体积分数按20%计算)。
工业上用硫铁矿为主要原料抽取硫酸,主要设备有沸腾米,接触室和吸引塔。
(1)硫铁矿在进入沸腾炉前需要粉碎,其目的是 。
(2)为了充分利用反应放出的热量,接触室中应安装 (填设备名称);吸引塔中填充许多瓷管,其作用是 。
(3)吸收塔排放的尾气中含有少量的SO![]() ,防止污染大气、充分利用原料,在排放前必须进行尾气处理并设法进行综合利用。
,防止污染大气、充分利用原料,在排放前必须进行尾气处理并设法进行综合利用。
传统的方法是:尾气中的SO![]() 通常用足量氨水吸收,然后再用稀硫酸处理,写出上述过程中的化学反应方程式: ,其优点是 。
通常用足量氨水吸收,然后再用稀硫酸处理,写出上述过程中的化学反应方程式: ,其优点是 。
创新方法是:将尾气中的SO![]() 用Na
用Na![]() SO
SO![]() 溶液吸收,然后再加热所得溶液,写出上述过程中的化学反应方程式: ,创新方法与传统方法相比,其优点是 。
溶液吸收,然后再加热所得溶液,写出上述过程中的化学反应方程式: ,创新方法与传统方法相比,其优点是 。
(4)在硫酸的工业制法中,下列生产操作及说法生产操作的主要原因二者都正确的是 (填序号)
A.从沸腾炉出来的炉气需净化,因为炉气中的SO![]() 与杂质反应
与杂质反应
B.硫酸生产中常采用高压条件,目的是提高SO![]() 的转化率
的转化率
C.SO![]() 被氧化为SO
被氧化为SO![]() 时需要使用催化剂,这样可以提高SO
时需要使用催化剂,这样可以提高SO![]() 的转化率
的转化率
D.SO![]() 用98.3%浓硫酸吸收,目的是防止形成酸雾,有利于SO
用98.3%浓硫酸吸收,目的是防止形成酸雾,有利于SO![]() 吸收完全
吸收完全
(5)某硫酸厂若要生产8吨98%的浓硫酸至少需要标准状况下的空气 m![]() ( O
( O![]() 空气中的体积分数按20%计算)。
空气中的体积分数按20%计算)。
工业上用硫铁矿为主要原料抽取硫酸,主要设备有沸腾米,接触室和吸引塔。
(1)硫铁矿在进入沸腾炉前需要粉碎,其目的是 。
(2)为了充分利用反应放出的热量,接触室中应安装 (填设备名称);吸引塔中填充许多瓷管,其作用是 。
(3)吸收塔排放的尾气中含有少量的SO ,防止污染大气、充分利用原料,在排放前必须进行尾气处理并设法进行综合利用。
,防止污染大气、充分利用原料,在排放前必须进行尾气处理并设法进行综合利用。
传统的方法是:尾气中的SO 通常用足量氨水吸收,然后再用稀硫酸处理,写出上述过程中的化学反应方程式: ,其优点是 。
通常用足量氨水吸收,然后再用稀硫酸处理,写出上述过程中的化学反应方程式: ,其优点是 。
创新方法是:将尾气中的SO 用Na
用Na SO
SO 溶液吸收,然后再加热所得溶液,写出上述过程中的化学反应方程式:
溶液吸收,然后再加热所得溶液,写出上述过程中的化学反应方程式:  ,创新方法与传统方法相比,其优点是 。
,创新方法与传统方法相比,其优点是 。
(4)在硫酸的工业制法中,下列生产操作及说法生产操作的主要原因二者都正确的是 (填序号)
A.从沸腾炉出来的炉气需净化,因为炉气中的SO 与杂质反应 与杂质反应 |
B.硫酸生产中常采用高压条件,目的是提高SO 的转化率 的转化率 |
C.SO 被氧化为SO 被氧化为SO 时需要使用催化剂,这样可以提高SO 时需要使用催化剂,这样可以提高SO 的转化率 的转化率 |
D.SO 用98.3%浓硫酸吸收,目的是防止形成酸雾,有利于SO 用98.3%浓硫酸吸收,目的是防止形成酸雾,有利于SO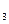 吸收完全 吸收完全 |
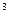 ( O
( O 空气中的体积分数按20%计算)。
空气中的体积分数按20%计算)。湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com