
题目列表(包括答案和解析)
| I1 | I2 | I3 | I4 | |
| C | 738 | 1451 | 7733 | 10540 |
| D | 577 | 1817 | 2745 | 11578 |
| 单键 | 双键 | 叁键 | ||
| AB | 键能(kJ?mol-1) | 357.7 | 798.9 | 1071.9 |
| 甲 | 键能(kJ?mol-1) | 154.8 | 418.4 | 941.7 |
 (4)E能与AB形成配合物,其中E提供
(4)E能与AB形成配合物,其中E提供A、B、C、D、E五种元素原子序数依次增大,A元素原子的价电子排列为ns2np2,B元素的最外层电子数是其电子层数的3倍,E元素原子的价电子排布为3d64s2。C、D的电离能数据如下(kJ?mol―1):
| I1 | I2 | I3 | I4 | |
| C | 738 | 1451 | 7733 | 10540 |
| D | 577 | 1817 | 2745 | 11578 |
(1)化合价是元素的一种性质。由C、D的电离能数据判断,C通常显 价,D显 价。
(2)某单质甲与化合物AB分子中电子总数相等,则甲分子中包含1个 键,2个 键。
(3)AB的总键能大于甲的总键能,但AB比甲容易参加化学反应。根据下表数据,说明AB比甲活泼的原因是 。
| 单键 | 双键 | 叁键 | ||
| AB | 键能/kJ?mol―1 | 357.7 | 798.9 | 1071.9 |
| 甲 | 键能/kJ?mol―1 | 154.8 | 418.4 | 941.7 |
(4)E能与AB形成配合物,其中E提供 ,AB提供 。
A、B、C、D四种短周期元素原子序数依次增大,A元素原子的价电子排列为ns2np2,B元素的最外层电子数是其电子层数的3倍,E元素原子的价电子排布为3d64s2。C、D的电离能数据如下(kJ·mol―1):
| I1 | I2 | I3 | I4 | |
| C | 738 | 1451 | 7733 | 10540 |
| D | 577 | 1817 | 2745 | 11578 |
(1)化合价是元素的一种性质。由C、D的电离能数据判断,C通常显 价,D显 价;
(2)某单质甲分子与化合物AB分子中电子总数相等,则甲分子中包含___个σ键,___个π键;
(3)AB的总键能大于甲的总键能,但AB比甲容易参加化学反应。根据下表数据,说明AB比甲活泼的原因是______________________________
| 单键 | 双键 | 叁键 | ||
| AB | 键能(kJ·mol―1) | 357.7 | 798.9 | 1071.9 |
| 甲 | 键能(kJ·mol―1) | 154.8 | 418.4 | 941.7 |
(4)E能与AB形成配合物,其中E提供______________,AB提供________________。
(5)下列晶胞中,阳离子与阴离子的个数为
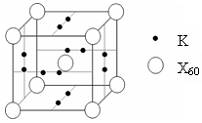
表中为一些短周期元素及相应氢化物沸点的数据:
元 素 性 质 | 元 素 编 号 | |||||
① | ② | ③ | ④ | ⑤ | ⑥ | |
氢化物的沸点(℃) | -60.7 | -33.4 | 100 | -87.7 | 19.54 | -84.9 |
最 高 化 合 价 | +6 | +5 | +5 | +7 | ||
最 低 化 合 价 | -2 | -3 | -2 | -3 | -1 | -1 |
A、B、Y均为上表中的元素。X是一种历史悠久,应用广泛的金属元素。
① X与Y可形成化合物XY、XY2, 二者可用接触法制强酸甲;
② A与B可形成化合物AB、AB2,二者均可用于制备强酸乙。
请回答:
(1)元素 ③ 氢化物的分子式是 __________。
(2)下列有关强酸甲、乙说法正确的是 ________。
a. 二者的浓溶液在常温时均可用铁制或铝制的容器贮运
b. 二者的浓溶液在敞口容器中放置,质量都会变化
c. 工业生产强酸甲、乙时,都要用水吸收相应的氧化物
d. 二者的稀溶液均是强氧化剂
(3)工业生产强酸甲时可用浓氨水处理尾气,并获得某种铵盐。
化学方程式为__________________________________。
(4)写出工业生产强酸乙时获得AB的化学方程式: 。
(5)工业生产强酸乙时可用纯碱溶液处理尾气,该反应如下:
AB + AB2 + Na2CO3 = 2 ![]() + CO2
+ CO2
① 在方框内填某盐的化学式
② 每产生44.8 L(标准状况)CO2,被吸收尾气的质量是 ______g。
(6) 表中属于第三周期的元素是_______________(用表中元素编号填写)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com