
甲、乙、丙、丁是由前20号元素组成的物质,有如下转化:甲+乙→丙+丁
(1)若甲为块状固体,丙为分子内同时具有极性键和非极性键可燃性气体,乙为水,则丙的结构式
H-C≡C-H
H-C≡C-H
.
(2)若甲和丁是同主族元素组成的单质,乙为水.且甲的组成元素位于第三周期,反应的离子方程式
2Na+2H2O=2Na++2OH-+H2↑
2Na+2H2O=2Na++2OH-+H2↑
.
(3)霍夫曼根据上述反应,用右图实验装置测定了氨分子的组成.打开分液漏斗活塞,滴下浓氨水至不再反应为止;关闭活塞,待恢复至室温,打开止水夹,试管内液面上升至2/3处.①滴加浓氨水后试管内的现象
产生大量白烟,黄绿色气体消失
产生大量白烟,黄绿色气体消失
②相应的反应化学方程式
8NH3+3Cl2=N2+6NH4Cl
8NH3+3Cl2=N2+6NH4Cl
(4)若甲Cl
2,乙为NH
4Cl反应,丁为HCl,丙为氮的氯化物,当消耗6.72L Cl
2(标状)时得到0.10mol氮的氯化物,丙的化学式
NCl3
NCl3
,反应方程式
3Cl2+NH4Cl═NCl3+4HCl
3Cl2+NH4Cl═NCl3+4HCl
(5)某短周期金属元素的单质与核电荷数为其2倍的金属元素的氧化物之间也能发生上述反应,请写出相应的化学方程式
2Al+3FeO
Al
2O
3+3Fe或4Al+2Fe
2O
32Al
2O
3+4Fe或8Al+3Fe
3O
44Al
2O
3+9Fe
2Al+3FeO
Al
2O
3+3Fe或4Al+2Fe
2O
32Al
2O
3+4Fe或8Al+3Fe
3O
44Al
2O
3+9Fe
.

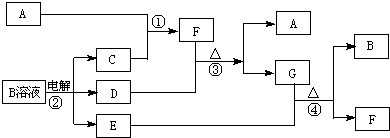
 甲、乙、丙、丁是由前20号元素组成的物质,有如下转化:甲+乙→丙+丁
甲、乙、丙、丁是由前20号元素组成的物质,有如下转化:甲+乙→丙+丁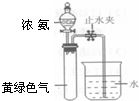 (2011?怀柔区模拟)甲、乙、丙、丁是由短周期元素组成的物质,反应如下:甲+乙→丙+丁
(2011?怀柔区模拟)甲、乙、丙、丁是由短周期元素组成的物质,反应如下:甲+乙→丙+丁