
题目列表(包括答案和解析)
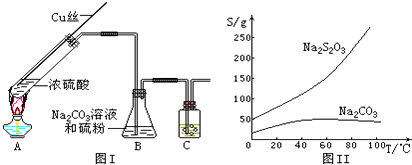
| 实验操作 | 预期现象与结论 |
| 步骤1:取适量“滤液”于小烧杯中,用滴管向小烧杯加入过量l mol/L BaCl2溶液. | 若出现白色浑浊,溶液可能存在SO32-. |
| 步骤2:将小烧杯中的浊液过滤、洗涤,将所得固体、滤液分别置于试管A、B备用. | / |
| 步骤3:向试管A中加入 |
|
| 步骤4:向试管B中加入 |
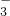 =CO2↑+HSO
=CO2↑+HSO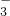
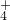 +OH-=NH3?H2O
+OH-=NH3?H2O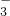 =CaCO3↓+CO
=CaCO3↓+CO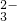 +2H2O
+2H2O +2Ba2++4OH-=AlO
+2Ba2++4OH-=AlO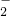 +2BaSO4↓+2H2O
+2BaSO4↓+2H2OA.向氢氧化钠溶液中通入过量CO2:2OH-+CO2====![]() +H2O
+H2O
B.硫酸铝溶液中加入过量氨水:Al3++4 NH3·H2O====![]() +4
+4![]() +2H2O
+2H2O
C.用石墨作电极电解饱和食盐水:2Cl-+2H2O![]() 2 OH-+H2↑+Cl2↑
2 OH-+H2↑+Cl2↑
D.氢氧化亚铁溶于足量稀硝酸:Fe(OH)2+2H+====Fe2++2H2O
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com