某化学兴趣小组在实验室利用氯气与石灰乳【Ca(OH)
2】制取漂白粉.
已知2Cl
2+2Ca(OH)
2═CaCl
2+Ca(ClO)
2+2H
2O
该兴趣小组设计了下列实验装置,进行如下实验:
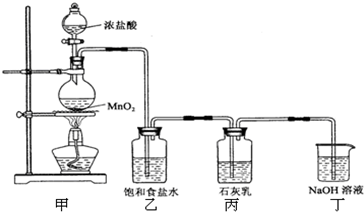
请回答下列问题:
(1)实验室用甲装置用于制备氯气,其反应的化学方程式是
MnO
2+4HCl(浓)
MnCl
2+Cl
2↑+2H
2O
MnO
2+4HCl(浓)
MnCl
2+Cl
2↑+2H
2O
;
(2)工业上电解饱和食盐水来制备氯气,其化学方程式是
;
(3)乙装置的作用是
除去Cl2中混有的HCl气体
除去Cl2中混有的HCl气体
,丁装置的作用是
进行尾气处理
进行尾气处理
.
(4)该兴趣小组用足量的浓盐酸与8.7g MnO
2制备氯气,并将所得氯气与过量的石灰乳反应,则理论上最多可制得Ca(ClO)
27.15
7.15
g.但小组成员发现,实际上产物中Ca(ClO)
2的质量明显小于理论值.为了探究其原因,小组成员查阅了相关资料得到:氯气和碱的反应为放热反应;温度较高时,氯气和碱还能发生如下反应:6Cl
2+6Ca(OH)
2 5CaCl
2+Ca(ClO
3)
2+6H
2O
(5)为了提高Ca(ClO)
2的产率,可对丙装置作适当改进.请你给出一种改进方法:
将丙装置置于装有冷水的容器中
将丙装置置于装有冷水的容器中
.

