硝苯吡啶(心痛定)是治疗心血管疾病的一种重要药物,其合成路线如下:
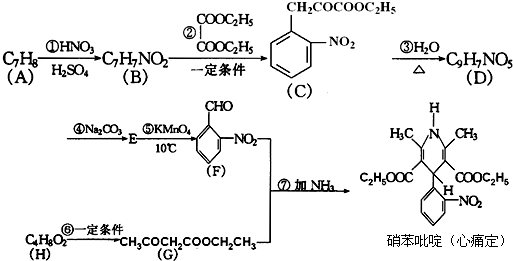
请回答下列问题:
(1)硝苯吡啶(心痛定)的化学式为
C19H22N2O6
C19H22N2O6
.
(2)指出反应②的反应类型:
取代反应
取代反应
.
(3)写出反应③的化学方程式:
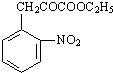
+H
2O
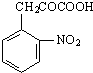
+C
2H
5OH

+H
2O

+C
2H
5OH
.
(4)方程式②和方程式⑥有一定的相似性,且含同一种产物,请写出(H)的结构简式
CH3COOC2H5
CH3COOC2H5
.写出反应⑥的方程式:
2CH
3COOC
2H
5CH
3COCH
2COOC
2H
5+C
2H
5OH
2CH
3COOC
2H
5CH
3COCH
2COOC
2H
5+C
2H
5OH
(5)H的同分异构体在一定条件下能与氢氧化钠溶液反应,则符合该条件的H的同分异构体有
5
5
种(不包含H本身).G的一种链状结构的同分异构体的核磁共振氢谱中只有2个吸收峰,其结构简式为
CH3CH2-CO-O-CO-CH2CH3或CH3-CO-CH2-O-CH2-CO-CH3
CH3CH2-CO-O-CO-CH2CH3或CH3-CO-CH2-O-CH2-CO-CH3
(任写一种).
(6)反应②是一种重要的酰基化反应,高中阶段也有一种酰基化反应----阿司匹林的制备,阿司匹林产品中通常含有一定的杂质(杂质不与酸反应),通常采用返滴定法测定阿司匹林片剂中乙酰水杨酸的含量.现称取10片该产品(设总质量为w
总g),研细混匀后,准确称取一定量(Gg)药粉于锥形瓶中,加入V
1mL(过量)的NaOH标准溶液[浓度c(NaOH) mol?L
-1],于水浴上加热使乙酰基水解完全后,再用HCl标准溶液[浓度c(HCl) mol?L
-1]回滴,以酚酞为指示剂,耗去HCl溶液V
2 mL.请列出求算每片药中含有乙酰水杨酸的质量(g/片)的计算式:
| [c(NaOH)V1-c(HCl)V2]×180.2 |
| 1000G |
×| [c(NaOH)V1-c(HCl)V2]×180.2 |
| 1000G |
×.
已知:①乙酰水杨酸溶于过量NaOH溶液的离子方程式可表示为:
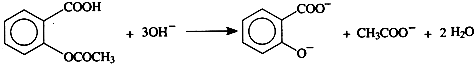
②乙酰水杨酸的摩尔质量为180.2g?mol
-1,水杨酸的pKa
l=3.0,pKa
2=13.1,乙酸的pKa=4.75 pKa=-lgKa.


 +H2O
+H2O +C2H5OH
+C2H5OH +H2O
+H2O +C2H5OH
+C2H5OH
![]()

![]() 已知乙酰水杨酸可溶于NaOH溶液中,并生成水杨酸盐和乙酸盐。其溶解反应式可表示为:
已知乙酰水杨酸可溶于NaOH溶液中,并生成水杨酸盐和乙酸盐。其溶解反应式可表示为:![]()

![]() 乙酰水杨酸的摩尔质量为180.2g?mol-1,水杨酸的pKal=3.0,pKa2=13.1,乙酸的pKa=4.75
乙酰水杨酸的摩尔质量为180.2g?mol-1,水杨酸的pKal=3.0,pKa2=13.1,乙酸的pKa=4.75