
题目列表(包括答案和解析)
| 化合物 | 甲 | 乙 | 丙 |
| 各元素原子个数比 | n(A):n(C)=2:1 | n(A):n(C)=1:1 | n(B):n(A)=1:4 |
| 化合物 | 丁 | 戊 | 己 |
| 各元素原子个数比 | n(D):n(B):n(C)=2:1:3 | n(E):n(F)=1:3 | n(B):n(F)=1:4 |
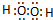
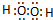


根据下列各题所给出的数据,得出的结论错误的是( )
| A.同温同压下,VLCO和H2的混合气体,完全燃烧消耗O2的体积为0.5VL |
| B.4.2g氮气和4.8g某单质RX所含原子个数相同,且分子个数之比为1:1,则R的相对原子质量为16 |
C.已知某氢氧化钠溶液中Na+与H2O的个数之比为1∶a,则可求出此溶液中氢氧化钠的质量分数为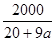 % % |
| D.将98g H2SO4溶于 1 L水中,则所制得的H2SO4溶液的物质的量浓度为1 mol/L |
| 元素 | 有关信息 |
| X | 元素主要化合价为-2,原子半径为0.074nm |
| Y | 所在主族序数与所在周期序数之差为4 |
| Z | 原子半径为0.102nm,其单质在X的单质中燃烧,发出明亮的蓝紫色火焰 |
| D | 最高价氧化物对应的水化物,能电离出电子数相等的阴、阳离子 |
| E | 单质是生活中常见金属,其制品在潮湿空气中易被腐蚀或损坏 |
| ||
| ||
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com