
题目列表(包括答案和解析)
(16分)如图所示:在800 mL的大烧杯中放入碎纸屑,把盛有50 mL 0.50 mol·L-1盐酸的200 mL烧杯放到大烧杯中,两只烧杯间填满碎纸屑。用泡沫塑料板做成大烧杯盖,通过盖子插入一根玻璃搅拌器(末端呈半圆环的玻璃棒)和一只温度计,测定溶液的温度。迅速往盐酸溶液中加入50 mL 0.55 mol·L-1烧碱溶液,盖好,搅拌溶液,观察温度的变化。当温度保持稳定时,记录读数,取出装反应液的烧杯,倒出溶液,清洗干净,保持内外杯壁干燥。重复进行三次实验。用这一实验可以粗略测定中和热。
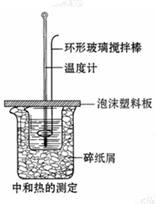
(1)烧杯间填满碎纸屑的作用是_____ 。
(2)要重复进行三次实验的目的是_____ 。
(3)烧杯如不盖硬纸板,求得的中和热数值将_____ (填“偏大”、“偏小”或“无影响”)。
(4)实验中若改用60 mL 0.50 mol·L-1盐酸和50 mL 0.55 mol·L-1烧碱溶液进行上述反应,与上述实验相比,所放出的热量_____ (填“相等”或“不相等”),所求中和热_____ (填“相等”或“不相等”),理由是_____。
(5)三次平行操作测得数据中,起始时盐酸与烧碱溶液温度相同,而终止温度与起始温度之差(t2-t1)分别为 ①2.3 ℃ ②2.4 ℃ ③2.9 ℃,则最终代入计算式的温度差的平均值为_____ ℃。
(1)开始时反应的速率大小为_____________。
(2)三试管中参加反应的锌的质量为_____________。
(3)反应终了,所需时间为_____________。
(4)在反应过程中,乙和丙中反应速率不同的理由是________________________(简要说明)。
如图所示:在800 mL的大烧杯中放入碎纸屑,把盛有50 mL 0.50 mol·L-1盐酸的200 mL烧杯放到大烧杯中,两只烧杯间填满碎纸屑.用泡沫塑料板做成大烧杯盖,通过盖子插入一根玻璃搅拌器(末端呈半圆环的玻璃棒)和一只温度计,测定溶液的温度.迅速往盐酸溶液中加入50 mL 0.55 mol·L-1烧碱溶液,盖好,搅拌溶液,观察温度的变化.当温度保持稳定时,记录读数,取出装反应液的烧杯,倒出溶液,清洗干净,保持内外杯壁干燥.重复进行三次实验.用这一实验可以粗略测定中和热.
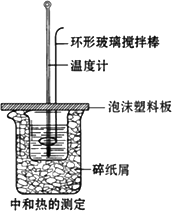
(1)烧杯间填满碎纸屑的作用是________.
(2)要重复进行三次实验的目的是________.
(3)烧杯如不盖硬纸板,求得的中和热数值将________(填“偏大”、“偏小”或“无影响”).
(4)实验中若改用60 mL 0.50 mol·L-1盐酸和50 mL 0.55 mol·L-1烧碱溶液进行上述反应,与上述实验相比,所放出的热量________(填“相等”或“不相等”),所求中和热________(填“相等”或“不相等”),理由是________.
(5)三次平行操作测得数据中,起始时盐酸与烧碱溶液温度相同,而终止温度与起始温度之差(t2-t1)分别为
①2.3℃
②2.4℃
③2.9℃,
则最终代入计算式的温度差的平均值为________℃.
目前市场上大量碳酸饮料、矿泉水、食用油等产品包装瓶几乎都是用PET(聚对苯二甲酸乙二醇脂,简称聚酯)制作的.某科学小组利用费聚酯饮料瓶制备对苯二甲酸.部分有机物的性质如下:
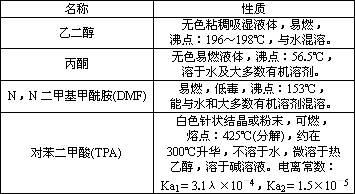
实验过程如下,试回答下列问题:
(1)对苯二甲酸的制备
①在100 mL四颈瓶上分别装置冷凝管、搅拌器和温度计.然后依次加入5.00g废饮料瓶碎片、0.05 g氧化锌、5 g碳酸氢钠和25 mL乙二醇.缓慢搅拌,油浴加热,将温度升至180℃(不超过185℃),在此温度下反应15分钟.
反应过程中的现象是________.
②冷却至160℃左右停止搅拌,将搅拌回流装置改成搅拌、减压蒸馏装置,减压蒸馏.这一步是为了分离出________.
③向四颈瓶中加入50 mL沸水,搅拌使四颈瓶中的残留物溶解.抽滤除去少量不溶物.抽滤需要用到的主要仪器有________.
④将滤液转移到400 mL烧杯中,用25 mL水荡洗滤瓶并倒入烧杯中,再添加水使溶液总体积达200 mL丙酮分2次洗涤,抽干,干燥.
(2)对苯二甲酸含量的测定
称取0.2000 g对苯二甲酸样品于250 mL烧杯中,加入30 mL DMF,搅拌溶解,加入10 mL蒸馏水,搅匀后加4滴酚酞指示剂,用0.1000 mol·L-1氢氧化钠标准溶液滴定,消耗氢氧化钠标准溶液体积为22.60 mL.
滴定终点的现象是________.
所测样品中对苯二甲酸的质量分数为________.
酸碱中和反应是中学化学一类重要的反应,其反应的本质都是H+和OH-反应生成H2O.某学生实验小组对课本中的两个酸碱中和实验进行了模拟研究.
(1)用下图装置进行强酸(50 mL 0.5 mol/L的HCI)和强碱(50 mL 0.55 mol/L的NaOH)反应的中和热测定.
①从实验装置上看,图中尚缺少的一种玻璃仪器是________;
②大小烧杯之间填满纸屑的作用是________;
③向组装好的量热器中加入50 mL盐酸并测定温度,取出温度计并冲
净后,再将已测定好温度的NaOH溶液50 mL加入量热器.下列加入50 mL NaOH溶液的操作正确的是________.
A.为了使酸碱充分中和,必须边滴加NaOH溶液边迅速搅拌
B.把50 mL NaOH溶液一次迅速倒入,盖上纸板迅速搅拌.
④若用醋酸代替上述盐酸实验,实验测得的中和热值________(填偏大、偏小或无影响).
(1)、用实验室准确配制的0.100 mol/L的NaOH溶液测定某未知浓度的稀盐酸.
其具体实验步骤如下:
①取一支碱式滴定管下图中有两只滴定管~上端未画出,你选择哪一只?________(填写对应字母),用少量标准NaOH溶液润洗2~3次水洗后的碱式滴定管,再加入标准的0.100 mol/L的NaOH溶液并记录液面刻度读数;
②用酸式滴定管精确的放出25.00 mL待测盐酸,置于用蒸馏水洗净的锥形瓶中,再加入酚酞(变色范围:8.2~10.0)试液2滴;
③滴定时,边滴边振荡,同进注视眼睛注视锥形瓶内容也颜色的变化,当锥形瓶内溶液由________(填写颜色变化)且半分钟内不褪色时,即达到滴定终点;
④记录液面刻度读数.根据滴定管的两次读数得出消耗标准盐酸的体积,再重复测定两次,实验结果记录见下表:

测得未知稀盐酸的物质的量浓度为________(保留小数点后3位).
⑤如果滴定结束时俯视碱式滴定管刻度读数(其它操作均正确),则对滴定结果~稀盐酸浓度的影响是________(填“偏高”、“偏低”或“无影响”).
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com