
题目列表(包括答案和解析)
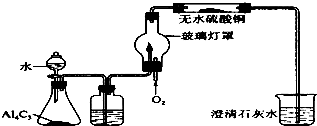
已知Al4C3+12H2O![]() 4Al(OH)3+3CH4↑某学习小组在实验室利用如图所示装置制取甲烷,并验证甲烷的组成.
4Al(OH)3+3CH4↑某学习小组在实验室利用如图所示装置制取甲烷,并验证甲烷的组成.

(1)洗气瓶中盛的溶液为________,作用________.
(2)验纯后在玻璃尖嘴处点燃甲烷,发现火焰呈黄色,与老师课上讲的“纯净的甲烷在空气中安静地燃烧,产生淡蓝色的火焰”不符,你认为原因是________.
(3)为了验证甲烷的组成元素为碳和氢,将燃着的导管套入玻璃灯罩内,如图所示,则证明甲烷中含有碳、氢元素的现象分别是________、________
(4)若将洗气瓶去掉,换成一段导管,则能否证明甲烷中含有碳、氢元素?________.
 已知Al4C3+12H2O═4Al(OH)3+3CH4↑某学习小组在实验室利用如图所示装置制取甲烷,并验证甲烷的组成.
已知Al4C3+12H2O═4Al(OH)3+3CH4↑某学习小组在实验室利用如图所示装置制取甲烷,并验证甲烷的组成. (1)写出用硝酸制取一氧化氮的离子方程式________________________。
(2)查资料得知,HCOOH![]() CO↑+H2O。实验室有如图甲所示的装置,制取一氧化碳可选用的装置为_________(填序号)。
CO↑+H2O。实验室有如图甲所示的装置,制取一氧化碳可选用的装置为_________(填序号)。
(3)查资料得知,利用催化剂可使汽车尾气中的一氧化碳和氮氧化物大部分发生反应转化为二氧化碳和氮气。该小组在实验室模拟汽车尾气处理,设计了如图乙所示装置(部分夹持和装置已略去)。

甲

乙
①实验前关闭旋塞K,先通氮气排净装置中的空气,其目的是______________________。
②装置(Ⅲ)的主要作用是_______________________________________________________。
③加热停止后,打开旋塞K,放入适量氧气时,装置(Ⅱ)中可观察到的现象是__________
____________________________________________________________________。
④该套装置中有不完善之处,还应在装置(Ⅳ)后补充_______________________________。
(4)工业上通常用氢氧化钠溶液吸收一氧化氮、二氧化氮的混合气体。相关反应为2NO2+2NaOH![]() NaNO3+NaNO2+H2O和NO2+NO+2NaOH
NaNO3+NaNO2+H2O和NO2+NO+2NaOH![]() 2NaNO2+H2O。将体积比为
2NaNO2+H2O。将体积比为![]() 的混合气体通入足量的氢氧化钠溶液中,气体完全反应后,所得溶液中
的混合气体通入足量的氢氧化钠溶液中,气体完全反应后,所得溶液中![]() __________________。
__________________。
I、某化学课外活动小组对污染大气的部分非金属氧化物进行探究。请根据题目要求回答下列问题。
(1)写出用硝酸制取NO的离子方程式 。
(2)查资料得知,HCOOH CO+H2O。实验室有如图l所示的装置,制取CO气体可选用的装置为
CO+H2O。实验室有如图l所示的装置,制取CO气体可选用的装置为
(填序号),实验室利用该装置还可制取的常见气体有 (写一种气体的分子式)。
(3)查资料得知,利用催化剂可使汽车尾气中的一氧化碳和氮氧化物大部分发生反应转化为二氧化碳和氮气。该小组在实验室模拟汽车尾气处理,设计了如图2所示装置(部分夹持和装置已略去)。


①实验前,关闭旋塞K,先通氮气排净装置中的空气,其目的是 。
②装置(III)的主要作用是 。
③该套装置中有不完善之处,还应在装置(Ⅳ)后补充 装置。
II、该课外小组设计的从ZnSO4、FeCl3的混合溶液中制取ZnSO4·7H2O过程如下:
a.在混合液中加入6 mol/L NaOH溶液,至pH=8为止。
b.过滤后得到沉淀,用蒸馏水多次洗涤沉淀。
c.向洗涤后的沉淀中加入2 mol/L的硫酸,保持溶液的pH在4~6,加热煮沸,趁热过滤,滤液即为ZnSO4溶液。
d.滤液中加入2 mol/L的硫酸,使其pH=2。
已知部分阳离子以氢氧化物的形式开始沉淀至完全沉淀时溶液的pH见下表,回答下列问题:
|
沉淀物 |
Fe(OH)3 |
Zn(OH)2 |
|
pH |
1.5~3.2 |
6.4~8.0 |
(1)步骤b中如何检测沉淀已经洗涤干净 。
(2)步骤d中加入硫酸,使其pH=2的目的是 ;要制得ZnSO4·7H2O的步骤d还缺少的操作是 ,所用的主要硅酸盐仪器是 。
I、某化学课外活动小组对污染大气的部分非金属氧化物进行探究。请根据题目要求回答下列问题。
(1)写出用硝酸制取NO的离子方程式 。
(2)查资料得知,HCOOH CO+H2O。实验室有如图l所示的装置,制取CO气体可选用的装置为
CO+H2O。实验室有如图l所示的装置,制取CO气体可选用的装置为
(填序号),实验室利用该装置还可制取的常见气体有 (写一种气体的分子式)。
(3)查资料得知,利用催化剂可使汽车尾气中的一氧化碳和氮氧化物大部分发生反应转化为二氧化碳和氮气。该小组在实验室模拟汽车尾气处理,设计了如图2所示装置(部分夹持和装置已略去)。

①实验前,关闭旋塞K,先通氮气排净装置中的空气,其目的是 。
②装置(III)的主要作用是 。
③该套装置中有不完善之处,还应在装置(Ⅳ)后补充 装置。
II、该课外小组设计的从ZnSO4、FeCl3的混合溶液中制取ZnSO4·7H2O过程如下:
a.在混合液中加入6 mol/L NaOH溶液,至pH=8为止。
b.过滤后得到沉淀,用蒸馏水多次洗涤沉淀。
c.向洗涤后的沉淀中加入2 mol/L的硫酸,保持溶液的pH在4~6,加热煮沸,趁热过滤,滤液即为ZnSO4溶液。
d.滤液中加入2 mol/L的硫酸,使其pH=2。
已知部分阳离子以氢氧化物的形式开始沉淀至完全沉淀时溶液的pH见下表,回答下列问题:
| 沉淀物 | Fe(OH)3 | Zn(OH)2 |
| pH | 1.5~3.2 | 6.4~8.0 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com