
题目列表(包括答案和解析)
某工厂用FeCl3溶液腐蚀镀有铜的绝缘板生产印刷电路(已知发生的反应为 2FeCl3 + Cu =2FeCl2 + CuCl2)。课外活动小组为确认生产后的废液的组成,进行如下实验:
(1)取100 mL废液加入足量的AgNO3溶液,生成沉淀 86.1g。
(2)另取100 mL废液放入铜片充分反应,铜片质量减少了2.56 g。
下列关于原废液组成的判断错误的是
A.c(Fe2+)︰c(Fe3+)︰c(Cu2+) = 2︰1 ︰1
B.c(Fe2+)︰c(Cu2+) = 2︰1
C.一定含有Fe 2+、Fe 3+、Cu2+、Clˉ
D.c(Clˉ) =" 6mol" / L,c(Fe 2+) =" 1.2mol" / L
(12分)下面是某化学研究性学习小组对某水样成分的检验过程,已知该水样中只可能含有K+、Mg2+、Ca2+、Cl-、CO和SO中的若干种,该小组同学取100 mL水样进行实验: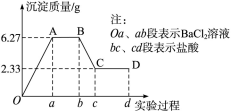
向样品中先滴加BaCl2溶液,再滴加1.0 mol·L-1的盐酸,实验过程中沉淀质量的变化如右图所示:
请回答下列问题:
(1)水样中一定含有的阴离子是________________,其物质的量之比为________。
(2)写出BC段曲线所表示反应的离子方程式________________。
(3)由B点到C点变化过程中消耗盐酸的体积为________。
(4)试根据实验结果推测K+是否存在?________(填“是”或“否”);若存在,K+的物质的量浓度c(K+)的范围是________。(若K+不存在,则不必回答该问)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com