
题目列表(包括答案和解析)
工业上氨气的制取是在高温、高压和催化剂的条件下进行的,并且该反应属于可逆反应,即该反应达到一定限度后,就会在反应物、产物浓度上保持一种动态的平衡(即化学平衡).
(1)请你填写下表中的空白
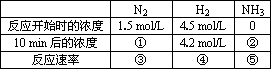
(2)比较是一种重要的化学学习方法.请用比较的方法归纳上表中反应速率与化学方程式中的计量系数的关系:________.
| ||
| △ |
| ||
| △ |
| ||
| 高温高压 |
 2NH3,该反应在固定容积的密闭容器中进行.下列各项标志着该反应达到化学平衡状态的是______(填序号)
2NH3,该反应在固定容积的密闭容器中进行.下列各项标志着该反应达到化学平衡状态的是______(填序号)

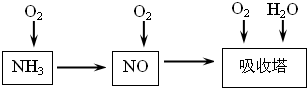
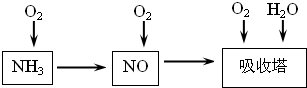
硫酸工业、硝酸工业和合成氨工业是重要的化学工业。
⑴在①硫酸工业②合成氨工业③硝酸工业三大工业中,在生产过程中有化学平衡存在的工业是 ,采用循环操作的是 。(填序号)
⑵过磷酸钙是一种常见的化肥,其有效成份是磷酸二氢钙,则工业上用磷酸钙制取过磷酸钙的化学方程式为 。
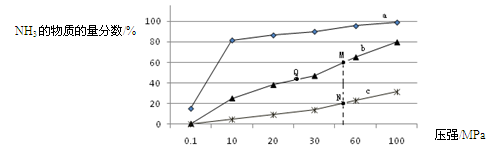
⑶合成氨生产中,根据化学平衡原理来确定的条件或措施有 (填写序号)。
A.氮气的制取 B.使用铁触媒作催化剂
C.使用400~500℃的温度 D.及时分离生成的NH3
E.合成氨在高压下进行 F.制水煤气除去CO2
⑷工业上用接触法制硫酸,最后的产品是98%硫酸或20%发烟硫酸(含SO3质量分数为20%的硫酸),若98%硫酸表示为SO3•aH2O,20%发烟硫酸表示为SO3•bH2O,则a,b分别为:a=_________,b=___________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com