蛇纹石可以看作由MgO、Fe
2O
3、Al
2O
3、SiO
2组成.实验室以蛇纹石为原料制取水合碱式碳酸镁,已知:
| 氢氧化物 |
Fe(OH)3 |
Al(OH)3 |
Mg(OH)2 |
| 开始沉淀pH |
1.5 |
3.3 |
9.4 |
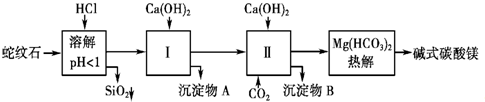
实验步骤如图甲:
请回答下列问题:
(1)操作①的名称
过滤
过滤
(2)检验溶液Ⅱ中是否含有Fe
3+的方程式 (最优方法)
Fe3++3SCN-=Fe(SCN)3
Fe3++3SCN-=Fe(SCN)3
(3)沉淀A与萤石(CaF
2)在硫酸酸化下可以制备石膏,写出反应方程式
2CaF2+2H2SO4+SiO2═2CaSO4+SiF4↑+2H2O
2CaF2+2H2SO4+SiO2═2CaSO4+SiF4↑+2H2O
(4)从沉淀混合物B中制取D,应加入一种试剂进行分离,其反应的离子方程式为
OH-+Al(OH)3═AlO2-+2H2O
OH-+Al(OH)3═AlO2-+2H2O
(5)操作②中应控制溶液pH的合理范围是
C
C
(填序号).
A.小于1.5B.1.5~3.3 C.7~8 D.大于9.4
(6)为探究所得的水合碱式碳酸镁[xMgCO
3?yMg(OH)
2?zH
2O]的组成,取样18.2g g于装置A的玻璃管中,请按由左-→右顺序将下列装置连接好(如图乙)(填序号,装置可重复使用):
C-→B-→A-→B-→D-→B(或D)
C-→B-→A-→B-→D-→B(或D)
,装置C应盛的试剂是
NaOH溶液
NaOH溶液
. 充分反应后,如果实验测得硬质玻璃管中剩余固体8.0g,共放出6.6gCO
2气体,则x:y:z=
3:1:3
3:1:3
.

 蛇纹石可以看作由MgO、Fe2O3、Al2O3、SiO2组成.实验室以蛇纹石为原料制取水合碱式碳酸镁,已知:
蛇纹石可以看作由MgO、Fe2O3、Al2O3、SiO2组成.实验室以蛇纹石为原料制取水合碱式碳酸镁,已知: