
题目列表(包括答案和解析)
实验室可用硫化氢通人碘粉末的悬浊液制取一定浓度的氢碘酸。其主要装置如图所示,所用的试剂有:稀盐酸;用ott0法压成的硬方块形CaS;碘在水中的悬浊液;NaOH溶液;NaHS饱和溶液。
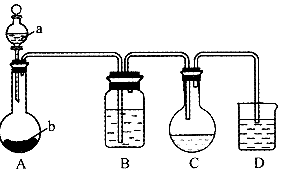
(1)在仪器中盛有的试剂:A中的a为 ,A中的b为 ,B为 ,D为 。
(2)C中反应完全时,应呈现的现象是什么?
(3)D中的导气管末端是否应插入液面以下?请说明理由。
(4)氢碘酸在溶质的质量分数为57%时,可形成“恒沸点”溶液,在125~127℃沸腾出的蒸气中为57%的HI。试设计用C中液体制取57%的氢碘酸的主要方法。
(5)氢碘酸在空气中发雾,应保存于封得很严的暗色瓶中。为防止HI的氧化,在密封之前最好采用的措施是什么?(发挥你的创见)
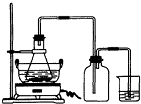 (2009?广东模拟)绿矾(FeSO4?7H2O)是重要的化学化工试剂,工业上常利用机械加工行业产生的废铁屑为原料制备.请回答下列问题:
(2009?广东模拟)绿矾(FeSO4?7H2O)是重要的化学化工试剂,工业上常利用机械加工行业产生的废铁屑为原料制备.请回答下列问题:| 序号 | 反应物用量 | 产品质量 |
| 1 | n(H2SO4):n(Fe)>1:1 | 介于Ⅰ级~Ⅱ级之间 |
| 2 | n(H2SO4):n(Fe)<1:1 | 优于Ⅰ级 |
| A、甲<乙<丙<丁 | B、丁<甲<乙=丙 | C、甲=丁<乙=丙 | D、丁<甲<乙<丙 |
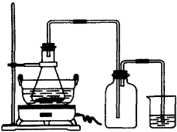 绿矾(FeSO4?7H2O)是重要的化学化工试剂,工业上常利用机械加工行业产生的废铁屑为原料制备.
绿矾(FeSO4?7H2O)是重要的化学化工试剂,工业上常利用机械加工行业产生的废铁屑为原料制备.| 序号 | 反应物用量 | 产品质量 |
| 1 | n(H2SO4):n(Fe)>1:1 | 介于Ⅰ级~Ⅱ级之间 |
| 2 | n(H2SO4):n(Fe)<1:1 | 优于Ⅰ级 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com