
题目列表(包括答案和解析)
在某个容积为2 L的密闭容器内,在T1℃时按下图1所示发生反应:
mA(g)+nB(g) ![]() pD(g)+qE(s),DH<0(m、n、p、q为最简比例的整数)。
pD(g)+qE(s),DH<0(m、n、p、q为最简比例的整数)。

(1)据图1所示,反应开始至达到平衡时,用D表示该反应速率为_____________;
(2)该反应的化学平衡常数K的表达式为________________________________;
(3) 下列措施能增大B的转化率的是 ( )
A.升高温度
B.保持体积不变通入1molB
C.保持体积不变移出部分物质D(g)
D.将容器的容积增大为原来2倍
E. 保持体积不变通入1mol A
(4) 反应开始时向容器中通入一定量的A和B,反应达到平衡时,测得D的浓度为0.6 mol.L-1 。(图2中纵坐标为D的浓度)
①请用实线在下图坐标系中该表示平衡的建立过程。
②若该反应在T2℃(T2> T1)温度下进行,请用虚线画出该平衡的建立过程。

某溶液中含有K+、NH+4、Al3+、OH-、AlO-2、SO2-4、CO2-3、SiO2-3、Cl-等离子中的某几种。现进行如下实验:①取少量溶液逐滴加入盐酸,先无明显现象,当盐酸加到一定体积后开始产生沉淀并逐渐增多,在沉浣不再增加后又产生一种无色气体,在气体不再产生后沉淀开始溶解,直至最后完全消失;
②取①所得溶液,加入Ba(OH)2溶液,无明显现象。
(1)原溶液中肯定存在的离子是 ;肯定不存在的离子是 。
(2)已知用一定体积的原溶液进行实验①时,需消耗0.2 mol/L的盐酸5 mL,这时向所得溶液中加入足量的硝酸银溶液可得沉淀0.187g,则原溶液中 (填“有”“没有”或“不确定”)Cl-。
下表是某食用碘盐包装袋上的部分说明:
| 配 料 | 食盐、碘酸钾、抗结剂 |
| 碘含量 | 35±15mg/kg |
| 储藏方法 | 密封、避光、防潮 |
| 食用方法 | 烹饪时,待食品熟后加入碘盐 |
(1)下列说法正确的是
A.高温会导致碘的损失
B.碘酸钾可氧化氯化钠
C.只用淀粉就能检验碘盐中的碘酸钾
D.该碘盐中碘酸钾含量为20~50mg/kg
(2)碘酸钾在工业上可用电解法制取。以石墨和不锈钢为电极,以KI溶液为电解液,
在一定条件下电解,反应的方程式为KI + 3H2O![]() KIO3 + 3H2↑。则阳极电极反应式为
KIO3 + 3H2↑。则阳极电极反应式为
(3)碘酸钾与碘化钾在酸性条件下发生如下反应,配平化学方程式,并标出电子转移的方向和数目。
KIO3+ KI+ H2SO4= K2SO4+ I2+ H2O
该反应的氧化剂为
(4)已知:I2+2S2O32-=2I-+S4O62-。某学生测定食用碘盐中碘的含量,其步骤为:
a.准确称取w g食盐,加适量蒸馏水使其完全溶解
b.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全
c.以淀粉为指示剂,逐滴加入物质的量浓度为2.0×10-3mol·L-1的Na2S2O3溶液10.0mL,恰好反应完全。则所测盐中碘的含量是(以含w的代数式表示) mg/kg。
(1)为了将空气装入气瓶内,现将一定质量的空气等温压缩,空气可视为理想气体。下列图象能正确表示该过程中空气的压强p和体积V关系的是 (填字母)。
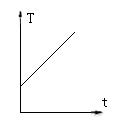
(2)质量一定的某种理想气体,在压强不变的条件下吸收热量的过程中,温度(T)随加热时间(t)变化关系如图所示。设单位时间所吸收的热量可看作不变。如果把压强不变的条件改为体积不变,则温度升高 (变快、变慢或快慢不变)
(3)空气在温度为300K,压强为1atm时的密度是1.0×10-3kg/L,当温度升高到400K,压强增大到2atm时,空气的密度为多少?

 甲乙两辆汽车在平直的公路上沿同一方向作直线运动,t=0时刻同时经过公路旁的同一个路标.在描述两车运动的 v-t图线中(如图所示),直线a、b分别描述了甲乙两车在0-20s 的运动情况.关于两车之间的位置关系,下列说法正确的是( )
甲乙两辆汽车在平直的公路上沿同一方向作直线运动,t=0时刻同时经过公路旁的同一个路标.在描述两车运动的 v-t图线中(如图所示),直线a、b分别描述了甲乙两车在0-20s 的运动情况.关于两车之间的位置关系,下列说法正确的是( )湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com