
题目列表(包括答案和解析)
中学常见物质A、B、D、E、G、M、Q之间有如下图所示变化关系(反应条件已省略):
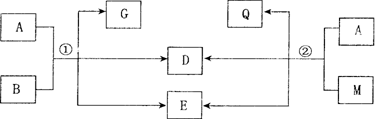
(1)若A是黑色非金属固体单质,G、Q、D是气体,E是水,D的化学式为________.
(2)若A是红色金属,B、M是同种溶质不同浓度的溶液,G、Q是气体,且G可通过化合反应生成Q.反应①的离子方程式是________.
(3)若A是Ca(OH)2,D是极易溶于水的气体.
①工业上合成D使用铁触媒作催化剂,采用500℃左右、20MPa-50MPa为生产条件的原因有________(填标号).
a.化学反应速率最大
b.催化剂的活性最大
c.反应物转化率最大
d.综合经济效益较好
上述反应中,每生成l mol D时放出热量46.2 kJ,该反应的热化学方程式是:
____________________________________
②当l mol Ca(OH)2分别与B、M完全反应时,反应①、②生成的D的物质的量之比为2∶1,B、M的化学式分别为________、________.
(1)AgNO3的水溶液呈 (填“酸”、“中”、“碱”)性,原因是(用离子方程式表示): ;
(2)氯化铝水溶液呈 性 ,(填“酸”、“中”、“碱”)性,原因是(用离子方程式表
示): ;
把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是 。
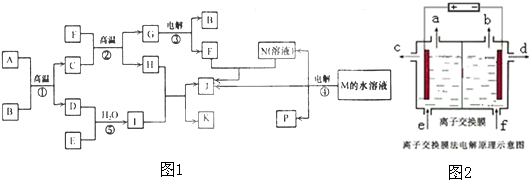
(3) 已知MgCl2·6H2O晶体在空气中加热时,释放部分结晶水,同时生成Mg(OH)Cl(碱式氯化镁)或生成MgO。下列是关于MgCl2·6H2O的综合应用:
![]()
![]()
![]()
![]()
![]() Mg(OH)2 MgO(耐火材料)
Mg(OH)2 MgO(耐火材料)
![]()
![]() MgCl2·6H2O
MgCl2·6H2O
![]()
![]()
![]() MgCl2 Mg
MgCl2 Mg
请回答下列问题:
①在上图的括号内应填的是在_______________环境中加热。
②Mg(OH)2固体存在如下溶解平衡:Mg(OH)2(固) ![]() Mg2++2OH-。向体系中加入(请填出两种不同类别的物质)_____________________________________________________ 有利于Mg(OH)2溶解。
Mg2++2OH-。向体系中加入(请填出两种不同类别的物质)_____________________________________________________ 有利于Mg(OH)2溶解。
③已知AnBm的离子积=c (Am+) n ·c (Bn-) m,式中c (Am+) n和c (Bn-) m表示离子的物质的量浓度,在室温时若测得Mg(OH)2饱和溶液的pH值为11,其离子积为___________________。
| 分解 |
| 还原 |
| 空气通入量/L?s-1 | 温度/℃ | SO2含量/% | SO3含量/% |
| 0.02 | 850 | 45.4 | 54.6 |
| 0.06 | 850 | 30.5 | 69.5 |
| 0.10 | 850 | 11.1 | 88.9 |
| 0.10 | 810 | 11.1 | 88.9 |
| 0.10 | 890 | 11.2 | 88.8 |
| ||
| ||



湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com