
题目列表(包括答案和解析)
A、B、C、D、E、F、G、H、I是元素周期表前四周期的元素,它们在元素周期中的位置如下图所示:

(1)B、C、D三种元素的第一电离能由大到小的顺序为 (用元素符号表示);
(2)有下列物质①CA3 ②GA3 ③EH ④JH ⑤FD2。请将这些物质的熔点由高到低排列 (填这些物质的序号),其中CA3 、GA3在常温、常压下都是气体,但CA3 比GA3 易液化,其主要原因是 。
(3)2007年诺贝尔化学奖获得者Gerhard Ertl利用光电子能谱证实:洁净L(可用于合成氨反应的催化剂)的表面上存在C原子,右图为C原子在L的晶面上的单层附着局部示意图(图中小黑色球代表C原子,灰色球代表L原子)。则在图示状况下,L颗粒表面上L/C原子数之比为 。

(4)A、B、C三种元素形成的一种化合物叫三聚氰胺(结构如图),由于其含氮量高被不法奶农添加到牛奶中来“提高”蛋白质的含量,造成全国许多婴幼儿因食用这种奶粉而患肾结石。三聚氰胺中二种环境的N原子的杂化形式分别是 。

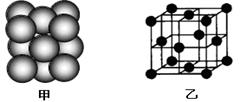
(5)M单质晶体中原子的堆积方式如下图甲所示,其晶胞特征如下图乙所示。

请回答:晶胞中M原子的堆积方式为 ,配位数为 。
A、B、C、D、E、F、G是原子序数依次增大的七种元素,其中A、B、C、D、E为短周期元素, F、G为第四周期元素。已知:A是原子半径最小的元素,B、C、D是紧邻的三个族的元素,C的三价阴离子和E的二价阳离子具有相同的电子层结构,F元素的基态原子具有六个成单电子,G是ⅠB族的元素。回答下列问题:
(1)写出E、F、G的元素符号 ,B、C、D元素的第一电离能由大到小的顺序是 (用元素符号表示),A元素分别与B、D元素形成的二种微粒都具有NH3相似的结构,属于等电子体,它们的化学式是 。
(2)F元素的原子基态价层电子排布图是 。
(3)向G的硫酸盐溶液中滴加氨水会生成蓝色沉淀,继续滴加氨水至沉淀刚好全部溶解时可得到蓝色溶液,继续向其中加入极性较小的乙醇可以生成深蓝色的[G(NH3)4]SO4·H2O沉淀。该深蓝色沉淀中的NH3通过________键与中心离子G2+结合;NH3分子中N原子的杂化方式是________;
(4)E单质晶体中原子的堆积模型如右图,晶胞是图中的 (填a、b或c);配位数是 ;若紧邻的四个E原子的中心连线构成的几何体的体积是a cm3,E单质的密度为ρg/ cm3;则E的相对原子质量的计算式是 。





(12分)有A、B、C、D、E、F六种元素,已知:它们位于三个不同的短周期,核电荷数依次增大;A与E、B与F分别同主族;A、E分别都能与D按原子个数1∶1或2∶1形成化合物;B、C分别能与D按原子个数1∶1或1∶2形成化合物。
(1)写出只含有A、B、D、E四种元素的两种无水盐的化学
式 、 。
(2)右图是A与D形成的一种化合物的晶体结构示意图,其中的虚线表示 。E与D按原子个数比1∶1形成的化合物的电子式为 。
(3)人们通常把拆开1mol某化学键所吸收的能量看成该化学键的键能。键能的大小可以衡量化学键的强弱,也可以用于估算化学反应的反应热(△H),化学反应的△H等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差。下表列出了上述部分元素形成的化学键的键能:
| 化学键 | F—D | F—F | B—B | F—B | B==D | D==D |
| 键能/ kJ·mol?1 | 460 | 176 | 347.7 | 347 | 745 | 497.3 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com