
题目列表(包括答案和解析)

 2SO3△H<0,下图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量.下列说法中正确的是______.
2SO3△H<0,下图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量.下列说法中正确的是______. 2SO3达到平衡后,SO3的体积分数为 a%,SO2的转化率为m.
2SO3达到平衡后,SO3的体积分数为 a%,SO2的转化率为m. 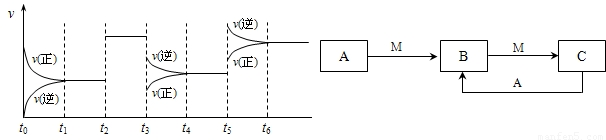
 2SO3△H<0,下图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量.下列说法中正确的是______.
2SO3△H<0,下图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量.下列说法中正确的是______. 2SO3达到平衡后,SO3的体积分数为 a%,SO2的转化率为m.
2SO3达到平衡后,SO3的体积分数为 a%,SO2的转化率为m. 下列各组物质中,所含氧原子数目相等的是 ( )
A、等体积的NO和CO B、等物质的量的SO2和SO3
C、等质量的O2和O3(臭氧) D、标准状况下的0.5 L CO2和1 L H2O
A.在25 ℃、1 atm下,等体积的N2O与CO2分子中所含电子数相等?
B.含有相同氧原子数目的SO2与H2O的质量相等?
C.常温下,等物质的量浓度的盐酸和醋酸中,氢离子浓度?相等??
D.在0 ℃、101 kPa时,1 mol SO3所占的体积为22.4 L
下列说法正确的是:
A、1mol任何物质的体积都是22.4L
B、等质量的SO2和SO3中所含的硫原子数相等
C、90g水相当于5mol水
D、22.4L氧气中一定含6.02×1023个氧分子
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com