
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
 гвЭМЮЊЪЕбщЪвФГХЈбЮЫсЪдМСЦПЩЯЕФБъЧЉЃЌЪдИљОнгаЙиЪ§ОнЛиД№ЯТСаЮЪЬтЃК
гвЭМЮЊЪЕбщЪвФГХЈбЮЫсЪдМСЦПЩЯЕФБъЧЉЃЌЪдИљОнгаЙиЪ§ОнЛиД№ЯТСаЮЪЬтЃКгвЭМЮЊЪЕбщЪвФГХЈбЮЫсЪдМСЦПЩЯЕФБъЧЉЃЌЪд ИљОнгаЙиЪ§ОнЛиД№ЯТСаЮЪЬтЃК
ИљОнгаЙиЪ§ОнЛиД№ЯТСаЮЪЬтЃК
ЃЈ1ЃЉИУХЈбЮЫсжаHClЕФЮяжЪЕФСПХЈЖШЮЊ mol/LЁЃ
ЃЈ2ЃЉШЁгУШЮвтЬхЛ§ЕФИУбЮЫсШмвКЪБЃЌЯТСаЮяРэСПжаВЛЫцЫљШЁЬхЛ§ЕФЖрЩйЖјБфЛЏЕФЪЧ ЁЃ
AЃЎШмвКжаHClЕФЮяжЪЕФСП BЃЎШмвКЕФХЈЖШ
CЃЎШмвКжаClЃЕФЪ§ФП  DЃЎШмвКЕФУмЖШ
DЃЎШмвКЕФУмЖШ
ЃЈ3ЃЉФГбЇЩњгћгУЩЯЪіХЈбЮЫсКЭеєСѓЫЎХфжЦ500 mLЮяжЪЕФСПХЈЖШЮЊ0.30 mol/LЯЁбЮЫсЁЃ
ЂйИУбЇЩњашвЊСПШЁ mLЩЯЪіХЈбЮЫсНјааХфжЦЁЃ
ЂкХфжЦЪБЃЌЦфе§ШЗЕФВйзїЫГађЪЧ(гУзжФИБэЪОЃЌУПИізжФИжЛФмгУвЛДЮ) ЁЃ
AЃЎгУ30 mLЫЎЯДЕгЩеБ2ЁЋ3ДЮЃЌЯДЕгвКОљзЂШыШнСПЦПЃЌЧсЧсвЁЖЏШнСПЦП
BЃЎгУСПЭВзМШЗСПШЁЫљашХЈбЮЫсЕФЬхЛ§ЃЌТ§Т§биББкзЂШыЪЂгаЩйСПЫЎЃЈдМ30 mLЃЉЕФЩеБжаЃЌгУВЃСЇАєТ§Т§НСЖЏЃЌЪЙЦфЛьКЯОљдШ
CЃЎНЋвбРфШДЕФбЮЫсбиВЃСЇАєзЂШы500 mLЕФШнСПЦПжа
DЃЎНЋШнСПЦПЕФВЃСЇШћИЧНєЃЌЕпЕЙвЁдШ
EЃЎИФгУНКЭЗЕЮЙмМгЫЎЃЌЪЙШмвКАМУцЧЁКУгыПЬЖШЯпЯрЧа
FЃЎМЬајЭљШнСПЦПФкаЁаФМгЫЎЃЌжБЕНвКУцНгНќПЬЖШЯп1ЁЋ2 cmДІ
ЂлдкХфжЦЙ§ГЬжаЃЌЯТСаВйзїЛсЪЙЫљХфжЦЕФЯЁбЮЫсЮяжЪЕФСПХЈЖШЦЋИпЕФЪЧ ЁЃ
AЃЎгУСПЭВСПШЁХЈбЮЫсЪБИЉЪгЙлВьАМвКУц
BЃЎШмвКзЂШыШнСПЦПЧАУЛгаЛжИДЕНЪвЮТОЭНјааЖЈШн
CЃЎЖЈШнЪБбіЪгПЬЖШЯп
DЃЎдкХфжУЧАгУвбжЊХЈЖШЕФЯЁбЮЫсШѓЯДШнСПЦП
ЃЈ4ЃЉЯжНЋ200 mL 0.30 mol/LЕФбЮЫсгы50 mL 0.80 mol/L CaCl2ШмвКЛьКЯ(ЬхЛ§БфЛЏКіТдВЛМЦ)ЃЌЫљЕУШмвКжаClЃЕФЮяжЪЕФСПХЈЖШЪЧ mol/LЃЛЯђЫљЕУЛьКЯШмвКжаМгШы5.3 g Na2CO3ЙЬЬхЃЌГфЗжЗДгІКѓЃЌШмвКжаЩњГЩГСЕэЕФжЪСПга_________gЁЃ
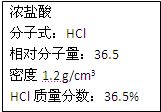
ЃЈ5ЃЉдкБъзМзДПіЯТЃЌНЋ______________L HClЦјЬхШмгк1000 mLЫЎжа(ЫЎЕФУмЖШЮЊ1 g/cm3)ЃЌЫљЕУбЮЫсЕФУмЖШЮЊ1.2 g/cm3ЃЌШмжЪжЪСПЗжЪ§ЮЊ36.5% ЁЃ(БЃСєаЁЪ§ЕуКѓвЛЮЛ)
(5Зж)дкБъзМзДПіЯТЃЌНЋ44.8LHClШмгк927mLЫЎ(УмЖШЮЊ1g/cm3)жаЃЌЫљЕУбЮЫсЕФУмЖШЮЊ1.05g/cm3ЃЌМЦЫуЫљЕУбЮЫсЕФШмжЪжЪСПЗжЪ§МАЮяжЪЕФСПХЈЖШЁЃ
(18Зж)ШчЯТЭМЫљЪОЃЌФГЭЌбЇЩшМЦвЛИіШМСЯЕчГиВЂЬНОПТШМюЙЄвЕдРэКЭДжЭЕФОЋСЖдРэЃЌЦфжаввзАжУжаXЮЊбєРызгНЛЛЛФЄЁЃ

ИљОнвЊЧѓЛиД№ЯрЙиЮЪЬтЃК
(1)ЭЈШыбѕЦјЕФЕчМЋЮЊ________(ЬюЁАе§МЋЁБЛђЁАИКМЋЁБ)ЃЌаДГіИКМЋЕФЕчМЋЗДгІЪН________________________________________________________ЁЃ
(2)ЬњЕчМЋЮЊ________(ЬюЁАбєМЋЁБЛђЁАвѕМЋЁБ)ЃЌЪЏФЋЕчМЋ(C)ЕФЕчМЋЗДгІЪНЮЊ________________________________________________________________________ЁЃ
(3)ЗДгІвЛЖЮЪБМфКѓЃЌввзАжУжаЩњГЩЧтбѕЛЏФЦжївЊдк________(ЬюЁАЬњМЋЁБЛђЁАЪЏФЋМЋЁБ)Чј
(4)ШчЙћДжЭжаКЌгааПЁЂвјЕШдгжЪЃЌБћзАжУжаЗДгІвЛЖЮЪБМфЃЌСђЫсЭШмвКХЈЖШНЋ________(ЬюЁАдіДѓЁБЁАМѕаЁЁБЛђЁАВЛБфЁБ)ЁЃ
(5)ШєдкБъзМзДПіЯТЃЌга2.24 LбѕЦјВЮМгЗДгІЃЌдђввзАжУжаЬњЕчМЋЩЯЩњГЩЕФЦјЬхЕФЗжзгЪ§ЮЊ________ЃЛБћзАжУжавѕМЋЮіГіЭЕФжЪСПЮЊ________ЁЃ
АйЖШжТаХ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com