
题目列表(包括答案和解析)
[化学——化学与生活]
下列内容都与人们的生活和健康密切相关,请根据要求填空:
(1)学生要注意合理膳食,注意食品的多样化,防止某种营养成分过多或过少。请回答下列问题:
①大米的主要成分在人体内最终变成了 (填名称)而被人体吸收。
②坏血病是由于缺乏维生素C而引起的,下列有关维生素C的说法正确的是 。
A.维生素C是脂溶性维生素,易在体内积存
B.维生素C可作食品添加剂
C.维生素C虽然被称为抗坏血酸,但![]() 它的水溶液并不呈酸性
它的水溶液并不呈酸性
![]() D.维生素C在水溶液中或受热时很容易被氧化,所以生吃新鲜蔬菜要比熟吃时维生素C的损失少
D.维生素C在水溶液中或受热时很容易被氧化,所以生吃新鲜蔬菜要比熟吃时维生素C的损失少
③蔬菜、水果中维生素C的含量较高,缺乏维生素C的同学在膳食中应该增加蔬菜、水果的摄入量,许多蔬菜、水果(如柠檬酸等)是 (填“酸性食物”或“碱性食物”)。
(2)下表是我国部分城市空气质量周报,阅读并回答下列问题:
| 城市 | 污染 指数 | 首要 污染物 | 空气质量级别 | 城市 | 污染 指数 | 首要[来源:Zxxk.Com] 污染物 | 空气质量级别 |
| 北京 | 92 | TSP | II | 济南 | 76 | TSP | II |
| 天津 | 82 | TSP | II | 武汉 | 83 | NOx | II |
| 哈尔滨 | 96 | TSP | II | 重庆 | 98 | SOx | II |
| 上海 | 74 | NOx | II | 长沙 | 61 | TSP | II |
| 注:TSP——空气中的飘尘 | |||||||
①最容易出现酸雨的城市是______;为减少城市酸雨的产生,可采取以下措施中的 。
A.禁止用煤作燃料
B.改善燃煤质量,限制高硫煤炭的开采
C.向已酸化的土壤中加石灰
D.调整和优化能源结构,加快开发和利用新能源。
②汽车尾气(含有CO、SO2与NO等物质)是城市空气的污染物,治理的方法之一是在汽车的排气管上装一个催化转换器,其特点是使CO与NO反应,生成可参与大气生态环境循环的无毒气体,写出CO与NO反应的化学方程式____________________________________________________________。
(3)水是生命之源,动植物的生命活动与其密切相关,回答下列问题:?
①工业废水中常含有不同类型的污染物,可采用不同的方法处理。以下处理措施和方法正确的是 。
| 选项 | 污染物 | 处理措施 | 方法类别 |
| A | 废酸 | 加氢氧化钠中和 | 中和法 |
| B | Cu2+等重金属离子 | 加硫酸盐沉降 | 沉淀法 |
| C | 含苯废水 | 用活性炭吸附 | 物理法 |
| D | 悬浮物 | 加明矾 | 混凝法 |
![]() ②我省湘江流域工厂较多,如果污水处理不当,容易造成工业污染。我国工业废水中几种污染物的最高允许排放浓度如下表:
②我省湘江流域工厂较多,如果污水处理不当,容易造成工业污染。我国工业废水中几种污染物的最高允许排放浓度如下表:
| 污染物 | 汞 | 镉 | 铅 |
| 主要存在形式 | Hg2+ | Cd2+ | Pb2+ |
| 最高允许排放浓度/(mg·dm-3) | 0.05 | 0.1 | 1.0 |
现有某工厂每日排放的污水中汞的质量分数为(1×10-6)%,镉的质量分数为(2×10-5)%,铅的质量分数为(5×10-5)%(设该污水的密度为1 g/cm3)。根据计算该厂三项污染物中 超标。
[化学——化学与生活](15分)
下列内容都与人们的生活和健康密切相关,请根据要求填空:
(1)学生要注意合理膳食,注意食品的多样化,防止某种营养成分过多或过少。请回答下列问题:
①大米的主要成分在人体内最终变成了 (填名称)而被人体吸收。
②坏血病是由于缺乏维生素C而引起的,下列有关维生素C的说法正确的是 。
A.维生素C是脂溶性维生素,易在体内积存
B.维生素C可作食品添加剂
C.维生素C虽然被称为抗坏血酸,但它的水溶液并不呈酸性
D.维生素C在水溶液中或受热时很容易被氧化,所以生吃新鲜蔬菜要比熟吃时维生素C的损失少
③蔬菜、水果中维生素C的含量较高,缺乏维生素C的同学在膳食中应该增加蔬菜、水果的摄入量,许多蔬菜、水果(如柠檬酸等)是 (填“酸性食物”或“碱性食物”)。
(2)下表是我国部分城市空气质量周报,阅读并回答下列问题:
| 城市 | 污染 指数 | 首要 污染物 | 空气质量级别 | 城市 | 污染 指数 | 首要 污染物 | 空气质量级别 |
| 北京 | 92 | TSP | II | 济南 | 76 | TSP | II |
| 天津 | 82 | TSP | II | 武汉 | 83 | NOx | II |
| 哈尔滨 | 96 | TSP | II | 重庆 | 98 | SOx | II |
| 上海 | 74 | NOx | II | 长沙 | 61 | TSP | II |
| 注:TSP——空气中的飘尘 | |||||||
 。
。| 选项 | 污染物 | 处理措施 | 方法类别 |
| A | 废酸 | 加氢氧化钠中和 | 中和法 |
| B | Cu2+等重金属离子 | 加硫酸盐沉降 | 沉淀法 |
| C | 含苯废水 | 用活性炭吸附 | 物理法 |
| D | 悬浮物 | 加明矾 | 混凝法 |
| 污染物 | 汞 | 镉 | 铅 |
| 主要存在形式 | Hg2+ | Cd2+ | Pb2+ |
| 最高允许排放浓度/(mg·dm-3) | 0.05 | 0.1 | 1.0 |
[化学——选修化学与生活](15分)麻醉剂的发现和使用,是人类医疗史上了不起的一项成就,它可使患者在接受治疗时感觉不到疼痛。
(1)笑气是人类最早应用于医疗的麻醉剂之一,它可由NH4NO3在微热条件下分解产生,产物除N2O外还有一种,此反应的化学方程式为______________________________,N2O也可以通过强还原性金属(如Mg)与稀HNO3反应制得,写出该反应的离子方程式
________________________________________。每生成标况下2.24l N2O,消耗HNO3的物质的量为_______________mol。
(2)另一种常用麻醉剂氯仿,常因保存不慎而被氧化,产生剧毒物光气(COCl2):![]() ,为了防止事故,使用前可用于检验氯仿是否变质的试剂是________________。
,为了防止事故,使用前可用于检验氯仿是否变质的试剂是________________。
A.淀粉一碘化钾溶液 B.NaOH溶液C.酚酞溶液 D.硝酸酸化的AgNO3溶液
(3)氯普鲁卡因盐酸盐是一种局部麻醉剂,麻醉作用较快,较强,毒性较低,其结构简式为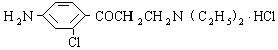 ,它可以以甲苯为原料合成
,它可以以甲苯为原料合成![]() ,其反应方程式为______________________________________,再经过________________反应(填反应类型)来合成
,其反应方程式为______________________________________,再经过________________反应(填反应类型)来合成![]() ,再经过一系列反应来合成。
,再经过一系列反应来合成。
(4)作为麻醉剂,氙气在医学上也生受重视,氙能溶于细胞质的油脂里,引起细胞的麻醉和膨胀,从![]() 而使神经末梢作用暂时停止。人们曾试用体积分数为80%的氙气和20%的氧气组成的混合气作为无副作用的麻醉剂。氙在元素周期表中位于___________周期,________族,此麻醉剂的平均式量为________。
而使神经末梢作用暂时停止。人们曾试用体积分数为80%的氙气和20%的氧气组成的混合气作为无副作用的麻醉剂。氙在元素周期表中位于___________周期,________族,此麻醉剂的平均式量为________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com