
题目列表(包括答案和解析)
孔林、孔庙、孔府是著名的旅游景点,近几年,修建的高速公路绕开了孔林、孔庙、孔府,以减少污染。你认为,在三孔景区,这样能有效减少的主要是( )
A﹒车辆排放的大量尾气 B﹒居民燃煤所产生SO2气体
C﹒车辆尘埃、生活垃圾 D﹒工厂所排“三废”
孔林、孔庙、孔府是著名的旅游景点,近几年,修建的高速公路绕开了孔林、孔庙、孔府,以减少污染。你认为,在三孔景区,这样能有效减少的主要是( )
A﹒车辆排放的大量尾气 B﹒居民燃煤所产生SO2气体
C﹒车辆尘埃、生活垃圾 D﹒工厂所排“三废”
| A、反应①②均为放热反应 | B、反应①②转移的电子数相同 | C、由反应①可推知:CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O(l)△H=-akJ?mol-1,a<574 | D、著用标准状况下4.48L CH4还原NO2至N2,放出的热量是173.4kJ |
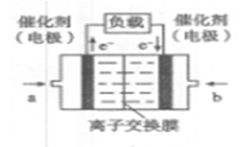
CO2是目前大气中含量最高的一种温室气体,控制和治理CO2是解决温室效应的有效途径。
(1)其中一种途径是将CO2转化成有机物实现碳循环。如:
2CO2(g)+2H2O(l)===C2 H4(g)+3O2(g) △H=十1411.0kJ/mol
2CO2(g) +3H2 O(l)=C2 H5OH(1)十3O2(g)△H = +1366.8kJ/mol
则由乙烯水化制乙醇反应的热化学方程式为 。
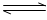
(2)在一定条件下,6H2(g)+2CO2(g) CH3CH2OH(g)+3H2O(g)。
CH3CH2OH(g)+3H2O(g)。
 温度(K) 温度(K)CO2转化率(%) n(H2)/n(CO2) | 500 | 600 | 700 | 800 |
| 1.5 | 45 | 33 | 20 | 12 |
| 2 | 60 | 43 | 28 | 15 |
| 3 | 83 | 62 | 37 | 22 |
 CH3OH(g)+H2O(g)。2min末该反应达到平衡,测得CH30H的浓度为0.2mol/L。下列判断不正确的是___ _。
CH3OH(g)+H2O(g)。2min末该反应达到平衡,测得CH30H的浓度为0.2mol/L。下列判断不正确的是___ _。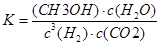
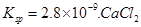 溶液与Na2CO3溶液混合可形成CaCO3沉淀,现将等体积的CaCl2溶液与Na2CO3溶液混合,若Na2CO3溶液的浓度为
溶液与Na2CO3溶液混合可形成CaCO3沉淀,现将等体积的CaCl2溶液与Na2CO3溶液混合,若Na2CO3溶液的浓度为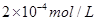 ,则生成沉淀所需CaCl2溶液的最小浓度为 。
,则生成沉淀所需CaCl2溶液的最小浓度为 。湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com