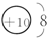认真阅读下面的新闻报道,完成后面的相关问题:
据某报2002年10月11日报道,2002年10月9日下午,某厂发生一起严重化学事故,该厂生产中需要无水苯作为溶剂,因此,使用苯前需要用金属钠除掉苯中的少量水分.在生产过程中,由于某种原因,误将1300kg甲苯当作苯投进一个反应釜中,并向反应釜中投入了10kg左右的金属钠.由于甲苯中含水量比苯少,金属钠不能被完全消耗掉,在反应釜四壁还残留有5kg左右的金属钠.
由于金属钠很活泼,遇水即发生剧烈反应,危险性极大.该反应釜严重威胁着该厂和周围群众的安全.经过众专家研究后,提出了三种处理事故的建议:
Ⅰ.打开反应釜,用工具将反应釜内的金属钠取出来;
Ⅱ.向反应釜中加水,通过化学反应“除掉”金属钠;
Ⅲ.采用远程滴加乙醇的方法向反应釜内加入乙醇,并设置放气管,排放乙醇与金属钠反应放出的气体和热量.
专家们进行了周密的研究和部署,经过紧张作业,至第二天晚8时,险情终于安全排除.
(1)文中提到“该反应釜严重威胁着该厂和周围群众的安全”,试用你学过的知识及题目所给信息解释危险性到底在哪里?
金属钠很活泼,遇水即发生剧烈反应
金属钠很活泼,遇水即发生剧烈反应
.
最终专家选择了最安全、最合理的解决问题的办法,你认为选择的是哪种方案?简要说明理由.
选用(3)乙醇与金属钠可以反应且比较温和
选用(3)乙醇与金属钠可以反应且比较温和
.
(2)分析文中信息可以知道,苯在工业生产中的一种重要用途是
作溶剂
作溶剂
苯
不能
不能
(填“能”或“不能”)与金属钠反应,等质量甲苯中的含水量大约是苯中含水量的
50%
50%
(填百分数).用金属钠可以除去苯中含有的水,而且也可以检验苯中是否含有水.那么应该用
无水CuSO4
无水CuSO4
(填化学试剂的化学式)检验乙醇中是否含有水.
(3)写出乙醇与金属钠的反应方程式:
2Na+2C2H5OH→H2↑+2C2H5ONa
2Na+2C2H5OH→H2↑+2C2H5ONa
(4)甲苯上的一个氢原子被氯原子取代可得到物质A,结构为

,物质B是它的同分异构体,也含有苯环,那么物质B可能的结构有
.

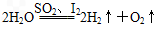 ,其循环过程分三步进行:
,其循环过程分三步进行: 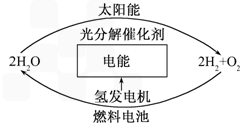
 ,物质B是它的同分异构体,也含有苯环,那么物质B可能的结构有
,物质B是它的同分异构体,也含有苯环,那么物质B可能的结构有