(2010?柳州三模)某同学为了测定三聚氰胺的分子式和结构简式,设计了如下实验:

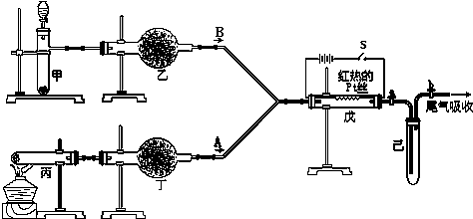
查阅资料:三聚氰胺的相对分子质量为126,三聚氰胺在常温下呈晶体,在加热条件下能与氧气发生反应生成二氧化碳、氮气和水.取12.6g的三聚氰胺晶体按如图装置进行实验(假设三聚氰胺完全反应转化成产物).
(1)写出A装置中发生反应的化学方程式
2Na
2O
2+2H
2O=4NaOH+O
2↑或2H
2O
22H
2O+O
2↑
2Na
2O
2+2H
2O=4NaOH+O
2↑或2H
2O
22H
2O+O
2↑
(一个即可).
(2)D装置能不能与E装置互换?
不能
不能
(填“能”或“不能”).
(3)当B装置中反应完全发生后,读取G中水的体积的实验操作顺序为
②③①
②③①
.(填序号)
①读数 ②冷却至室温 ③调平F、G装置中的液面
(4)测定数据如下:
| 装置 |
D |
E |
| 实验前 |
101.0g |
56.0g |
| 实验后 |
106.4g |
69.2g |
经测定,F中收集的气体折合标准状况下的体积为6.72L.
①利用上述实验数据,计算三聚氰胺的实验式为
CN2H2
CN2H2
.
②三聚氰胺的分子式为
C3N6H6
C3N6H6
.
③若C装置选用下列材料代替铜网,可选用
C
C
(填序号)
A.CuO B.Mg C.Ag D.C
(5)已知氰酸(HCN)的结构简式为H-C≡N,氰胺的结构简式为H
2N-C≡N,三聚氰胺分子中每个原子最外层电子数均达到8电子或2电子结构,试写出其结构简式:
.
(6)三聚氰胺分子中所有原子
否
否
(填是、否)共平面.





 某同学设计了如图所示装置(夹持仪器省略)进行系列实验,实验时将药品A逐滴加入到固体B中,请根据下列实验回答问题:
某同学设计了如图所示装置(夹持仪器省略)进行系列实验,实验时将药品A逐滴加入到固体B中,请根据下列实验回答问题: