
题目列表(包括答案和解析)
(13分) 实验室用氯化钠固体配制1![]() 的NaCl溶液0.5L,回答下列问题:
的NaCl溶液0.5L,回答下列问题:
(1)请写出该实验的实验步骤:
①计算,② ,③ ,④ ,⑤洗涤,⑥ ,⑦摇匀。
用托盘天平(指针向上的)称量样品时,若指针偏向右边,则表示( )
A、左盘重,样品轻 B、左盘轻,砝码重
C、右盘重,砝码轻 D、右盘轻,砝码重
需要NaCl g,实际用托盘天平称量的质量是 g。
(2)所需仪器除托盘天平,还需要哪些玻璃仪器才能完成该实验,请写出: 、 、 、 。
使用容量瓶前必须进行的操作是 。
(3)从该溶液中取出50mL,其中NaCl的物质的量浓度为 。
(13分) 实验室用氯化钠固体配制1 的NaCl溶液0.5L,回答下列问题:
的NaCl溶液0.5L,回答下列问题:
(1)请写出该实验的实验步骤:
①计算,② ,③ ,④ ,⑤洗涤,⑥ ,⑦摇匀。
用托盘天平(指针向上的)称量样品时,若指针偏向右边,则表示( )
A、左盘重,样品轻 B、左盘轻,砝码重
C、右盘重,砝码轻 D、右盘轻,砝码重
需要NaCl g,实际用托盘天平称量的质量是 g。
(2)所需仪器除托盘天平,还需要哪些玻璃仪器才能完成该实验,请写出: 、 、 、 。
使用容量瓶前必须进行的操作是 。
(3)从该溶液中取出50mL,其中NaCl的物质的量浓度为 。
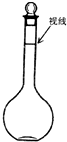 实验室用氯化钠固体配制1.00mol/L的NaCl溶液0.5L,回答下列问题
实验室用氯化钠固体配制1.00mol/L的NaCl溶液0.5L,回答下列问题湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com