
题目列表(包括答案和解析)


分析下面氧化还原反应中化合价变化关系,用双线桥标出电子转移方向和数目,并在横线上回答指定问题。
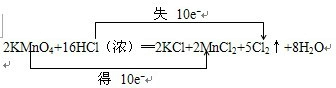
(1) 2KMnO4+16HCl=2KCl+2MnCl2+5Cl2+8H2O (双线桥法表示2分)
氧化剂 ,还原剂 ,该反应中盐酸既表现 性,又表现 性。
(2)(2分)当有2. 5mol Cl2生成时,转移 mol电子

| |||||||||||
(8分)(1)已知离子反应: +6I—+6H+=R—+3I2+3H2O,n=_____,R元素在
+6I—+6H+=R—+3I2+3H2O,n=_____,R元素在 中的化合价是___ __。
中的化合价是___ __。
(2)化学实验中,如使某步中的有害产物作为另一步的反应物,形成一个循环,就可不再向环境排放该种有害物质。例如: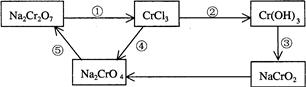
①在上述有编号的步骤中,需用还原剂的是_______,需用氧化剂的是 。 (填编号)。
②标出下面化学方程式电子转移的方向和数目(用双线桥表示),并回答有关问题
Na2Cr2O7+6KI+14HCl = 2CrCl3+2NaCl+6KCl+3I2+7H2O
反应中的还原剂___________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com