
题目列表(包括答案和解析)
(08山东海阳一中模拟)(14分)某校化学课外小组的同学为了探究碳酸钠和碳酸氢钠两种物质的性质,做了如下实验:实验I.如图A~D所示。
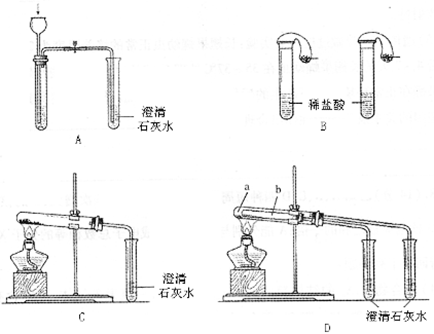
(1)若用实验D来验证碳酸钠和碳酸氢钠的热稳定性,则试管b中装入的固体最好是 ,实现现象是__。
(2)若用实验来鉴别碳酸钠和碳酸氢钠两种固体,能达到实验目的的是(填装置序号) 。
(3)若测定Na2CO3固体中混有的少量NaHCO3的质量分数,C能否达到实验目的?若能,请说明其计算所需的数据 ;若不能,请简要说明理由 。
实验II.将碳酸钠与碳酸氢钠溶液分别与澄清石灰水混合并充分反应。
(1)当石灰水过量时,反应的离子方程式分别为 、 。
(2)当碳酸氢钠与氢氧化钙物质的量之比为2:1时,所得溶液中溶质的化学式为 ,请设计实验检验所得溶液中溶质的阴离子 。
某化学课外小组的同学为了探究碳酸钠和碳酸氢钠两种物质的性质,做了如下实验:
实验Ⅰ.如图所示.
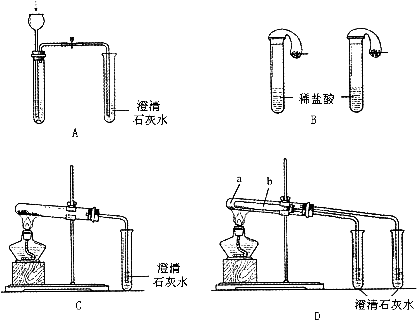
(1)若用实验D来验证碳酸钠和碳酸氢钠的热稳定性,则试管b中装入的固体最好是________,实现现象是________.
(2)若用实验来鉴别碳酸钠和碳酸氢钠两种固体,能达到实验目的的是(填装置序号)________.
(3)若测定Na2CO3固体中混有的少量NaHCO3的质量分数,C能否达到实验目的?若能,请说明其计算所需的数据)________;若不能,请简要说明理由______________________________.
实验Ⅱ.将碳酸钠与碳酸氢钠溶液分别与澄清石灰水混合并充分反应.
(1)当石灰水过量时,反应的离子方程式分别为________、________.
(2)当碳酸氢钠与氢氧化钙物质的量之比为2∶1时,所得溶液中溶质的化学式为_________,请设计实验检验所得溶液中溶质的阴离子________.
(6分)取22.1g碳酸钠和碳酸氢钠的混合粉末样品,将其分成两等份,取其中一份加热到质量不再改变,冷却后称其质量为7.95g;另一份溶于水,配成600mL溶液。试计算(计算结果用小数形式表示):
(1)原样品中碳酸钠的物质的量为多少?
(2)所配溶液中Na+的物质的量浓度为多少?
(6分)取22.1g碳酸钠和碳酸氢钠的混合粉末样品,将其分成两等份,取其中一份加热到质量不再改变,冷却后称其质量为7.95g;另一份溶于水,配成600mL溶液。试计算(计算结果用小数形式表示):
(1)原样品中碳酸钠的物质的量为多少?
(2)所配溶液中Na+的物质的量浓度为多少?
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com