2012年10月29日,超强飓风“桑迪”登陆美国东海岸,给人们的生命财产造成巨大损失.灾区人们的饮水必须用漂白粉等药品消毒后才能饮用,以防止传染病发生.
(1)试用化学方程式表示工业制取漂白粉的过程:
2Cl2+2Ca(OH)2=Ca(ClO)2+CaCl2+2H2O
2Cl2+2Ca(OH)2=Ca(ClO)2+CaCl2+2H2O
(2)已知浓盐酸和漂白粉中的成分之一次氯酸钙能发生如下反应:
Ca(ClO)
2+4HCl(浓)=CaCl
2+2Cl
2↑+2H
2O用贮存很久的漂白粉与浓盐酸反应制得的氯气中,可能含有的杂质气体是
A
A
.
①CO
2 ②HCl ③H
2O ④O
2A.①②③B.②③④C.②③D.①④
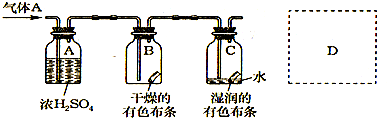
(3)某学生应用如图所示的方法研究物质的性质,其中气体A的主要成分是氯气,杂质是空气和水蒸气.回答下列问题:
①该项研究(实验)的主要目的是
比较Cl2和HClO谁有漂白性
比较Cl2和HClO谁有漂白性
;
②浓H
2SO
4的作用是
吸收气体中的水蒸汽
吸收气体中的水蒸汽
,与研究目的直接相关的实验现象是
B中的布条不褪色,C中的布条褪色
B中的布条不褪色,C中的布条褪色
;
③这样的实验设计还存在事故隐患,请在图中的D处画出能克服该缺陷的装置
.