
题目列表(包括答案和解析)

| |||||||||||||||||||

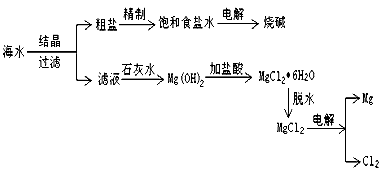
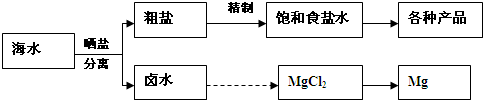
(1)在实验室进行过滤所需要的玻璃仪器为烧杯__________、__________;
(2)在粗盐中含有Ca2+、Mg2+、![]() 等杂质,精制时所用的试剂为:A.盐酸、B.氯化钡溶液、C.氢氧化钠溶液、D.碳酸钠溶液,则加入试剂的顺序是__________ (填序号);
等杂质,精制时所用的试剂为:A.盐酸、B.氯化钡溶液、C.氢氧化钠溶液、D.碳酸钠溶液,则加入试剂的顺序是__________ (填序号);
(3)电解饱和食盐水时,与电源正极相连的电极上发生的电极反应为__________________;与电源负极相连的电极附近溶液的pH__________ (填“变大”“变小”或“不变”);
(4)往Mg(OH)2中加入盐酸后,要获得MgCl2·6H2O晶体,需要进行的实验操作依次为__________ (填编号)。
A.蒸馏 B.灼烧 C.过滤 D.蒸发 E.冷却结晶
| ||
| ||
| ||
| ||
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com