(三选一)【化学——选修化学与技术】
下列反应对自然界中碳酸钙的搬运、喀斯特地貌的形成具有重要意义:CaCO3+H2O+CO2=Ca2+ +2HCO3-。富含二氧化碳的地下水流经大理石岩层时,通过该反应腐蚀岩层,久而久之,就形成了溶洞,溶洞还可能塌垮而形成天坑。地下河把Ca2+和HCO3-带到其他地方,渗出、滴下的水蒸发后,碳酸氢钙[Ca(HCO3)2]分解Ca(HCO3)2=CaCO3↓+H2O+CO2↑,产生的碳酸钙不断累积,就形成了钟乳石、石笋、石柱等自然景观。
(1)写出Na2CO3溶液中通入二氧化碳时反应的离子方程式:_______________ 据此,为什么除去二氧化碳气体中混有的少量氯化氢等酸性气体时,用饱和NaHCO3溶液而不用Na2CO3溶液_____________
(2)用NaOH溶液吸收二氧化碳气体,每摩尔氢氧化钠最多可吸收标准状况下__________升CO2。
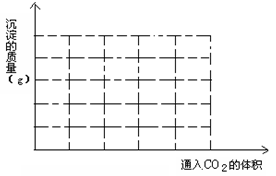
(3)向一定量的氢氧化钙溶液中慢慢通入二氧化碳气体,请在图中画出反应体系中沉淀的质量与通入二氧化碳体积之间的关系图