
题目列表(包括答案和解析)
下列说法正确的是
A、500℃、30MPa下,将0.5mol N2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为: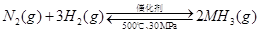 △H=-38.6kJ·mol-1
△H=-38.6kJ·mol-1
B、10mL 0.5mol/L CH3COONa溶液与6mL 1mol/L盐酸混合:c(Cl-)>c(CH3COOH) >c(Na+)>c(H+)>c(OH-)
C、实验测得环己烷(l)、环己烯(l)和苯(l)的标准燃烧热分别为-3916 kJ/mol、-3747 kJ/mol和-3265 kJ/mol,可以证明在苯分子中不存在独立的碳碳双键
D、在25℃下,将a mol·L-1的氨水与0.01 mol·L-1的盐酸等体积混合,反应时溶液中c(NH4+)=c(Cl—)。用含a的代数式表示NH3·H2O的电离常数Kb=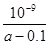
下列说法正确的是
A.中和相同体积、相同c(H+)的①硫酸、②盐酸和③醋酸所需相同浓度的NaOH溶液的体积关系:V1>V2=V3
B.将0.1 mol·L-1 CH3COOH溶液加水稀释,在此过程中,醋酸的电离程度、溶液的pH都逐渐增大
C.稀氨水中部分粒子的浓度大小关系: c(NH4+)>c(OH-)>c(H+)> c(NH3·H2O)
D.已知氢气的标准燃烧热为-285.8kJ·mol-1,相应的热化学方程式为
2H2(g) + O2(g)=2H2O(l) ΔH= –285.8kJ·mol-1
下列说法正确的是
A.中和相同体积、相同c(H+)的①硫酸、②盐酸和③醋酸所需相同浓度的NaOH溶液的体积关系:V1>V2=V3
B.将0.1 mol·L-1 CH3COOH溶液加水稀释,在此过程中,醋酸的电离程度、溶液的pH都逐渐增大
C.稀氨水中部分粒子的浓度大小关系: c(NH4+)>c(OH-)>c(H+)> c(NH3·H2O)
D.已知氢气的标准燃烧热为-285.8kJ·mol-1,相应的热化学方程式为
2H2(g) + O2(g)=2H2O(l) ΔH= –285.8kJ·mol-1
下列说法正确的是
A.中和相同体积、相同c(H+)的①硫酸、②盐酸和③醋酸所需相同浓度的NaOH溶液的体积关系:V1>V2=V3
B.将0.1 mol·L-1 CH3COOH溶液加水稀释,在此过程中,醋酸的电离程度、溶液的pH都逐渐增大
C.稀氨水中部分粒子的浓度大小关系: c(NH4+)>c(OH-)>c(H+)> c(NH3·H2O)
D.已知氢气的标准燃烧热为-285.8kJ·mol-1,相应的热化学方程式为
2H2(g) + O2(g)=2H2O(l) ΔH= –285.8kJ·mol-1
下列说法正确的是
A.中和相同体积、相同c(H+)的①硫酸、②盐酸和③醋酸所需相同浓度的NaOH溶液的体积关系:V1>V2=V3
B.将0.1 mol·L-1 CH3COOH溶液加水稀释,在此过程中,醋酸的电离程度、溶液的pH都逐渐增大
C.稀氨水中部分粒子的浓度大小关系: c(NH4+)>c(OH-)>c(H+)> c(NH3·H2O)
D.已知氢气的标准燃烧热为-285.8kJ·mol-1,相应的热化学方程式为
2H2(g) + O2(g)=2H2O(l) ΔH= –285.8kJ·mol-1
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com