
题目列表(包括答案和解析)
已知M2O7 x-+3S 2-+14H+=2 M3++3S↓+7H2O则M2O7 x-中的M的化合价为
A.+2价 B.+3价 C.+4价 D.+6价
第题(分)银制器皿久置会失去光泽,这并不是仅仅由于氧气的作用,是被“流动的水和游荡的风”所侵蚀,经分析,银器失去光泽是由于其表面形成了X ,X可由以下三种方法除去,从而使银器恢复光泽。
① 将银器置于盛有苏打水的铝制器皿中煮沸
② 将银器在KSCN或NH4SCN溶液中放置几分钟
③ 将银器用A的乙醇-水溶液处理数分钟,X与A反应的物质的量比为1:8,A是 NH4SCN的同分异构体,所有原子均只有一种化学环境。
试回答如下问题:
⑴ 给出X 和 A的化学式,并写出生成X的化学方程式
⑵ 写出除去X的三种方法的化学反应方程式
⑶ 计算X 在水中的溶解度,
已知Ksp,X = 6.3×10-50, X的阴离子对应的酸Ka1=9.5×10-8, Ka2=1.0×10-14
⑷ 试判断X在浓度相同的HNO3与HCl中的溶解性大小,说明你的理由
| 一定条件下 |
| H2O |
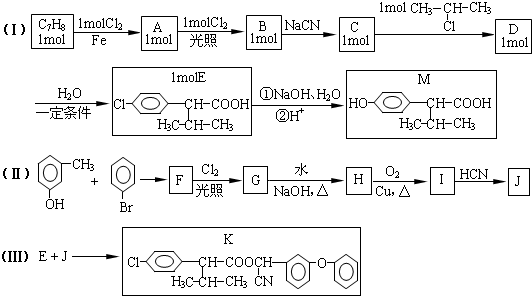
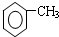 制备高分子化合物
制备高分子化合物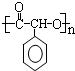 的合成路线流程图(无机试剂任选)
的合成路线流程图(无机试剂任选)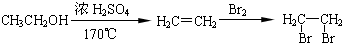
| 压强/MPa 转化率/% 温度/℃ |
0.1 | 0.5 | 1 | 10 |
| 400 | 99.2 | 99.6 | 99.7 | 99.9 |
| 500 | 93.5 | 96.9 | 97.8 | 99.3 |
| 600 | 73.7 | 85.8 | 89.5 | 96.4 |
| ||
| ||
| ||
| △ |
| ||
| △ |
| 开始沉淀时的pH | 沉淀完全时的pH | |
| Mg2+ | 9.6 | 11.0 |
| Ca2+ | 12.2 | c(OH-)=1.8mol?L-1 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com