
题目列表(包括答案和解析)
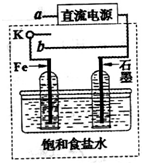 (2013?淄博二模)海水是丰富的资源宝库,从海水中提取元素是化学工业的重要组成部分.
(2013?淄博二模)海水是丰富的资源宝库,从海水中提取元素是化学工业的重要组成部分.| 除去悬浮 |
| 杂质 |
| 浓缩 |
| 氯化剂 |
| 氯化 |
| 热空气 |
| Na2CO3溶液 |
| 吸收 |
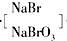
| H2SO4 |
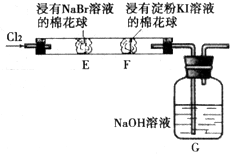 某化学小组用如图所示装置验证卤素单质氧化性的相对强弱.下列说法不正确的是( )
某化学小组用如图所示装置验证卤素单质氧化性的相对强弱.下列说法不正确的是( )湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com