
题目列表(包括答案和解析)
(A)【物质结构与性质】
有A、B、C、D、E、F六种元素,B原子得到一个电子后3p轨道全充满,A+比B原子形成的离子少一个电子层;C原子的p轨道半充满,形成的氢化物的沸点是同主族元素的氢化物中最低的;D和E是位于同一主族的短周期元素,E元素的最高化合价和最低化合价的代数和为零,E在其最高价氧化物中的质量分数为46.67%;F元素的核电荷数为26。
请回答下列问题:
(1)A元素位于元素周期表中第_________周期第_________族;F元素基态原子形成的+2价阳离子的电子排布式为_________。
(2)C与B形成的CB3分子中C原子的杂化方式是_______,其分子的空间形状是_______。
(3)另一元素X与A同主族,其第一电离能小于A,晶体XB与AB熔点较高的是_________,其理由是_______________________________________________________________。
(4)1 mol ED晶体中含有的E—D共价键的数目是_________。
(B)【实验化学】
阿司匹林(乙酰水杨酸)是由水杨酸和乙酸酐合成的:
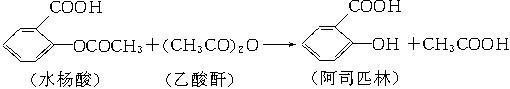
在生成乙酰水杨酸的同时,水杨酸分子之间也能发生聚合反应,生成少量聚合物(副产物)。合成乙酰水杨酸的实验步骤如下:
①向150 mL干燥锥形瓶中加入
②减压过滤,用滤液淋洗锥形瓶,直至所有晶体收集到布氏漏斗中。抽滤时用少量冷水洗涤晶体几次,继续抽滤,尽量将溶剂抽干。然后将粗产品转移至表面皿上,在空气中风干。
③将粗产品置于100 mL烧杯中,搅拌并缓慢加入25 mL 饱和碳酸氢钠溶液,加完后继续搅拌2—3 min,直到没有二氧化碳气体产生为止。过滤,用5—10 mL蒸馏水洗涤沉淀。合并滤液于烧杯中,不断搅拌,慢慢加入15 mL 4 mol·L-1盐酸,将烧杯置于冰水中冷却,即有晶体析出。抽滤,用冷水洗涤晶体1—2次,再抽干水分,即得产品。
请回答下列问题:
(1)第①步中,要控制温度在85—
(2)在第②步中,用冷水洗涤晶体,其目的是_________________________________________、__________________________________________。
(3)在第③步中,加入饱和碳酸氢钠溶液的作用是___________________________________,加入盐酸的作用是________________________________________。
(4)如何检验产品中是否混有水杨酸?___________________________________________
____________________________________________________________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com