
题目列表(包括答案和解析)
(14分)有甲、乙两位学生均想利用原电池反应检测金属的活动性顺序,两人均使用镁片和铝片作电极,但甲同学将电极放入6 mol/L H2SO4溶液中,乙同学将电极放入6 mol/L的NaOH溶液中,如下图: 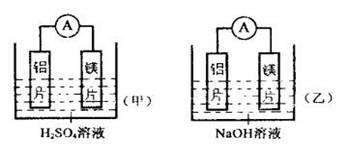
⑴写出甲池中负极的电极反应式 ;
⑵写出甲池中电极反应的总反应的离子方程式: 。
⑶如果甲与乙同学均认为“构成原电池的电极材料如果都是金属,则构成负极材料的金属应比构成正极材料的金属活泼”,则甲会判断出 活动性更强,而乙会判断出 活动性更强(填元素符号)。
⑷由此实验,可得到如下哪些正确结论? 。
A.利用原电池反应判断金属活动性顺序时应注意选择合适的介质(电解质)。
B. 该实验说明金属活动顺序表已过时,已没有实用价值。
C. 该实验说明化学研究对象复杂、反应受条件影响较大,因此应具体问题具体分析。
D. 镁的金属性不一定比铝的金属性强。
(5)美国阿波罗宇宙飞船上使用了一种新型装置,其构造如右图所示:a、b两个电极均由多孔的碳块组成。它是将 能转化为 能的装置。b电极为电池的 极,生成的水可以作为航天员的饮用水,当生成90克水时,转移的电子的物质的量是 mol。
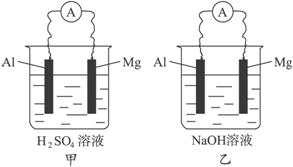
(1)写出甲池中正极的电极反应式:____________________________________________。
(2)写出乙池中负极的电极反应式:____________________________________________。
总反应的离子方程式为_____________________________________________________。
(3)如果甲与乙同学认为“构成原电池的材料如果都是金属,则构成负极材料的金属应比构成正极材料的金属活泼”,则甲会判断出_________活泼性更强,而乙会判断出_________活泼性更强(写元素符号)
(4)由实验,可得到如下哪些正确的结论( )
A.利用原电池反应判断金属活动性顺序时应注意选择合适的介质
B.镁的金属性不一定比铝的金属性强
C.该实验证明金属活动顺序表已过时,没有实用价值
D.该实验说明化学研究对象复杂,反应条件影响较大,因此应具体问题具体分析
(5)上述实验也反过来证明了“直接利用金属活动顺序表判断原电池中的正负极”这一种做法_________(填“可靠”或“不可靠”)。如不可靠,提出另一个判断原电池正负极的可行实验方案____________________________________________________________________(如可靠,可不填写)。
(14分)本世纪,人类社会将逐渐步入氢经济时代。目前大规模产氢方式仍是化学制氢。
I、催化重整制氢
以甲醇为例,反应制氢气的一般途径有:
CH3OH(l)=2H2(g)+CO(g) △H1=+128 kJ·mol-1
CH3OH(l)+H2O(l)=3H2(g)+CO2(g) △H2= a kJ·mol-1
已知:H2(g)+1/2O2(g)=H2O(l) △H=-286 kJ·mol-1
为求得△H2,还要知道 的燃烧热,若其燃烧热为△H=一283 kJ·mol-1,则△H2= 。
Ⅱ、金属置换制氢
(1)研究表明,刚切割的金属表面具有很高的反应活性。当铝或铝合金在水中被切割或碾碎的时候,可以持续地释放出氢气。使用铝与水反应制氢气比使用其它活泼金属与水反应制氢气的优点有:①价廉,成本较低;② 。
(2)利用天然气重整得到的CO、H2混合气对金属氧化物进行还原,然后将金属与水反应放出氢气,由此达成一个良性循环。根据高中所学的知识合理预测该金属单质,并写出该金属在加热的条件下与水蒸汽反应的化学方程式 。
III、太阳能制氢
利用光能分解水必须要有催化剂的参与。下列有关催化剂的说法正确的是
A.使用高效催化剂分解水制得H2的同时还可以获得能量
B.使用高效催化剂后常温下水可以自发分解
C.硅胶具有多孔结构,有较大的表面积,常用做催化剂的载体
D.对于可逆反应,催化剂在增大正反应速率的同时也增大逆反应速率
Ⅳ、配位氢化物制氢
在硼氢化钠(NaBH4)水溶液中加入特定催化剂后,可以迅速地发生水解反应生成偏硼酸钠和氢气。请写出此水解反应的化学方程式 。
将无水偏硼酸钠、氢化镁(MgH2)放入球磨设备中,通入氩气或氢气并保持压强100~500 kPa研磨0.5~4 h,即可得到硼氢化钠。研磨过程中需要通入氩气或氢气并保持压强100~500 kPa的目的是 。
本世纪,人类社会将逐渐步入氢经济时代。目前大规模产氢方式仍是化学制氢。
I、催化重整制氢
以甲醇为例,反应制氢气的一般途径有:
CH3OH(l)=2H2(g)+CO(g) △H1=+128 kJ·mol-1
CH3OH(l)+H2O(l)=3H2(g)+CO2(g) △H2= a kJ·mol-1
已知:H2(g)+1/2O2(g)=H2O(l) △H=-286 kJ·mol-1
为求得△H2,还要知道 的燃烧热,若其燃烧热为△H=一283 kJ·mol-1,则△H2= 。
Ⅱ、金属置换制氢
(1)研究表明,刚切割的金属表面具有很高的反应活性。当铝或铝合金在水中被切割或碾碎的时候,可以持续地释放出氢气。使用铝与水反应制氢气比使用其它活泼金属与水反应制氢气的优点有:①价廉,成本较低;② 。
(2)利用天然气重整得到的CO、H2混合气对金属氧化物进行还原,然后将金属与水反应放出氢气,由此达成一个良性循环。根据高中所学的知识合理预测该金属单质,并写出该金属在加热的条件下与水蒸汽反应的化学方程式 。
III、太阳能制氢
利用光能分解水必须要有催化剂的参与。下列有关催化剂的说法正确的是
A.使用高效催化剂分解水制得H2的同时还可以获得能量
B.使用高效催化剂后常温下水可以自发分解
C.硅胶具有多孔结构,有较大的表面积,常用做催化剂的载体
D.对于可逆反应,催化剂在增大正反应速率的同时也增大逆反应速率
Ⅳ、配位氢化物制氢
在硼氢化钠(NaBH4)水溶液中加入特定催化剂后,可以迅速地发生水解反应生成偏硼酸钠和氢气。请写出此水解反应的化学方程式 。
将无水偏硼酸钠、氢化镁(MgH2)放入球磨设备中,通入氩气或氢气并保持压强100~500 kPa研磨0.5~4 h,即可得到硼氢化钠。研磨过程中需要通入氩气或氢气并保持压强100~500 kPa的目的是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com