
题目列表(包括答案和解析)
下列反应的离子方程式,正确的是( )
A.Fe2O3溶于过量的氢酸碘中:Fe2O3+6H ====2Fe
====2Fe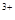 +3H2O
+3H2O
B.向NaAlO2溶液中通人过量CO2:AlO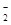 +CO2+2H2O====A1(OH)3↓+CO
+CO2+2H2O====A1(OH)3↓+CO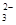
C.向漂白粉溶液中通人SO2气体:Ca +2C1O
+2C1O +SO2+H2O====CaSO3↓+2HClO
+SO2+H2O====CaSO3↓+2HClO
D.向Fe(NO3)2溶液中加人稀盐酸:3Fe +4H
+4H +NO
+NO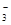 ====3Fe
====3Fe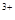 +NO↑+2H2O
+NO↑+2H2O
下列反应的离子方程式,正确的是( )
A.Fe2O3溶于过量的氢酸碘中:Fe2O3+6H![]() ====2Fe
====2Fe![]() +3H2O
+3H2O
B.向NaAlO2溶液中通人过量CO2:AlO![]() +CO2+2H2O====A1(OH)3↓+CO
+CO2+2H2O====A1(OH)3↓+CO![]()
C.向漂白粉溶液中通人SO2气体:Ca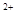 +2C1O
+2C1O +SO2+H2O====CaSO3↓+2HClO
+SO2+H2O====CaSO3↓+2HClO
D.向Fe(NO3)2溶液中加人稀盐酸:3Fe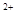 +4H
+4H +NO
+NO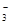 ====3Fe
====3Fe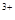 +NO↑+2H2O
+NO↑+2H2O
下列反应的离子方程式,正确的是( )
A.Fe2O3溶于过量的氢酸碘中:Fe2O3+6H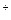 ====2Fe ====2Fe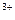 +3H2O +3H2O |
B.向NaAlO2溶液中通人过量CO2:AlO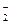 +CO2+2H2O====A1(OH)3↓+CO +CO2+2H2O====A1(OH)3↓+CO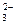 |
C.向漂白粉溶液中通人SO2气体:Ca +2C1O +2C1O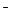 +SO2+H2O====CaSO3↓+2HClO +SO2+H2O====CaSO3↓+2HClO |
D.向Fe(NO3)2溶液中加人稀盐酸:3Fe +4H +4H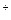 +NO +NO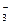 ====3Fe ====3Fe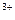 +NO↑+2H2O +NO↑+2H2O |
下列反应的离子方程式,正确的是( )
A.Fe2O3溶于过量的氢酸碘中:Fe2O3+6H![]() ====2Fe
====2Fe![]() +3H2O
+3H2O
B.向NaAlO2溶液中通人过量CO2:AlO![]() +CO2+2H2O====A1(OH)3↓+CO
+CO2+2H2O====A1(OH)3↓+CO![]()
C.向漂白粉溶液中通人SO2气体:Ca![]() +2C1O
+2C1O![]() +SO2+H2O====CaSO3↓+2HClO
+SO2+H2O====CaSO3↓+2HClO
D.向Fe(NO3)2溶液中加人稀盐酸:3Fe![]() +4H
+4H![]() +NO
+NO![]() ====3Fe
====3Fe![]() +NO↑+2H2O
+NO↑+2H2O

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com