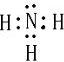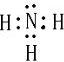已知A、B、C、D、E为五种短周期不同主族的元素,其原子序数依次递增.A、E两种原子最外层电子数之和是B原子最外层电子数的2倍;C、E两种原子最外层电子数之和是D原子最外层电子数的2倍.A、E形成的化合物甲分子中电子总数为18,D原子核外最外层电子排布式为ns
nnp
n+2.请回答下列问题
(1)B、C、D三种元素的第一电离能较大的是
N
N
(填写元素符号)
(2)A单质与C单质在一定条件下可化合为乙,室温下,向pH=a的乙的水溶液中加入等体积pH=b的甲的水溶液,且a+b=14,充分作用后,溶液的pH
>
>
7(填“>”“<”或“=”),该溶液中各种离子浓度由大到小的顺序为
c(NH4+)>C(Cl-)>c(OH-)>c(H+)
c(NH4+)>C(Cl-)>c(OH-)>c(H+)
.
(3)A、B两元素也可形成多种化合物,其中相对分子质量最小的分子为丙.用D的单质和丙可以构成原电池,电池用多孔的惰性电极浸入浓KOH溶液,在X极通入化合物丙,Y极通入D的单质,则X极的电极反应式为
CH4-8e-+10OH-=CO32-+7H20
CH4-8e-+10OH-=CO32-+7H20
.
(4)工业生产E元素单质的化学方程式为
.
(5)常温常压下,由A、B、D可组成液态物质J.现有2.3gJ与足量的D的单质充分反应,生成标准状况下2.24L BD
2气体和2.7gA
2D液体,同时放出68.35kJ的热量,该反应的热化学方程式为
C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(l)△H=-1367KJ/mol
C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(l)△H=-1367KJ/mol
.



 ,你认为
,你认为