
题目列表(包括答案和解析)
(16分)已知含有同一种元素的四种物质A、B、C、D 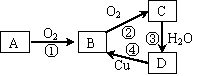 具有如右图所示的转化关系,其中A为单质,是工业上合成氨的重要原料,则:
具有如右图所示的转化关系,其中A为单质,是工业上合成氨的重要原料,则:
(1)单质A的电子式是 ,组成单质A的元素为X,X元素在周期表中位于第 周期 族,X的氢化物的结构式为 ,请写出合成该氢化物的反应的化学方程式为 。
(2)D物质的名称是 ,D物质的浓溶液经常会略带黄色,请用化学方程式表示其原因
(3)反应④中的还原剂是 ,请写出反应④的离子方程式 。
(4)生产、生活中B、C的大量排放会严重污染环境,任写一种B、C引起的环境问题
(5)如右图,将一盛有纯净干燥的气体C的试管倒立于水中,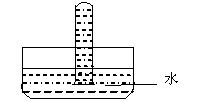 经过足够长的时间后,试管内水位上升的高度为试管高度的 ,若将盛有C 和O2混合气体的试管倒立于水中,经过足够长的时间后,试管内气体体积缩小为原体积的六分之一,则原混合气体中NO2和O2的体积比可能是 。
经过足够长的时间后,试管内水位上升的高度为试管高度的 ,若将盛有C 和O2混合气体的试管倒立于水中,经过足够长的时间后,试管内气体体积缩小为原体积的六分之一,则原混合气体中NO2和O2的体积比可能是 。
 已知A、B、C、D、E都是元素周期表中前四周期的元素,它们的核电荷数A<B<C<D<E.B原子的p轨道半充满,形成的氢化物的沸点是同主族元素的氢化物中最低的.D原子得到一个电子后3p轨道全充满.A+比D原子形成的离子少一个电子层.C与A形成A2C型离子化合物.E的原子序数为26,E原子或离子外围有较多能量相近的空轨道而能与一些分子或离子形成配合物.请根据以上情况,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)
已知A、B、C、D、E都是元素周期表中前四周期的元素,它们的核电荷数A<B<C<D<E.B原子的p轨道半充满,形成的氢化物的沸点是同主族元素的氢化物中最低的.D原子得到一个电子后3p轨道全充满.A+比D原子形成的离子少一个电子层.C与A形成A2C型离子化合物.E的原子序数为26,E原子或离子外围有较多能量相近的空轨道而能与一些分子或离子形成配合物.请根据以上情况,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示) 则:
则:


| ||
| ||



 已知A、B、C、D、E都是元素周期表中前四周期的元素,它们的核电荷数A<B<C<D<E.B原子的p轨道半充满,形成的氢化物的沸点是同主族元素的氢化物中最低的.D原子得到一个电子后3p轨道全充满.A+比D原子形成的离子少一个电子层.C与A形成A2C型离子化合物.E的原子序数为26,E原子或离子外围有较多能量相近的空轨道而能与一些分子或离子形成配合物.请根据以上情况,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)
已知A、B、C、D、E都是元素周期表中前四周期的元素,它们的核电荷数A<B<C<D<E.B原子的p轨道半充满,形成的氢化物的沸点是同主族元素的氢化物中最低的.D原子得到一个电子后3p轨道全充满.A+比D原子形成的离子少一个电子层.C与A形成A2C型离子化合物.E的原子序数为26,E原子或离子外围有较多能量相近的空轨道而能与一些分子或离子形成配合物.请根据以上情况,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com