
题目列表(包括答案和解析)
(方程式每空2分,其余每空1分,共21分。)氧化还原反应和离子反应是高一所学过的重要化学反应类型,仔细思考回答下列问题:
(Ⅰ)下列一组有水参与的反应:
①2Na + 2H2O =" 2NaOH" + H2↑
②2Na2O2 + 2H2O =" 4NaOH" + O2↑
③Na2O+ H2O ="2NaOH"
④3Fe+4H2O Fe3O4+4H2
Fe3O4+4H2
⑤2H2O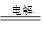 2H2↑+ O2↑
2H2↑+ O2↑
⑥2F2 + 2H2O =" 4HF" + O2
(1)其中不属于氧化还原反应的是 (填编号)
(2)在这些氧化还原反应中,水只作氧化剂的反应是 (填编号)
水只作还原剂的反应是 (填编号)水既作氧化剂,又作还原剂是 (填编号)
水既不作氧化剂,又不作还原剂是 (填编号)
(3)根据你的理解,氧化还原反应的实质是( )
| A.分子中的原子重新组合 | B.氧元素的得失 |
| C.电子的得失或共用电子对的偏移 | D.化合价的改变 |
(方程式每空2分,其余每空1分,共21分。)氧化还原反应和离子反应是高一所学过的重要化学反应类型,仔细思考回答下列问题:
(Ⅰ)下列一组有水参与的反应:
①2Na + 2H2O =" 2NaOH" + H2↑
②2Na2O2 + 2H2O =" 4NaOH" + O2↑
③Na2O+ H2O ="2NaOH"
④3Fe+4H2O Fe3O4+4H2
Fe3O4+4H2
⑤2H2O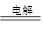 2H2↑+ O2↑
2H2↑+ O2↑
⑥2F2 + 2H2O =" 4HF" + O2
(1)其中不属于氧化还原反应的是 (填编号)
(2)在这些氧化还原反应中,水只作氧化剂的反应是 (填编号)
水只作还原剂的反应是 (填编号)水既作氧化剂,又作还原剂是 (填编号)
水既不作氧化剂,又不作还原剂是 (填编号)
(3)根据你的理解,氧化还原反应的实质是( )
A.分子中的原子重新组合 B.氧元素的得失
C.电子的得失或共用电子对的偏移 D.化合价的改变
(4)请你运用所学知识分析3NO2+H2O = 2HNO3+NO是否属于氧化还原反应? (填“是”或“不是”),若是,这个反应的氧化剂是 ,还原剂是 。
(Ⅱ)写出下列反应的离子方程式:
①往氯化铁溶液加入铁粉:
②过量二氧化碳通入澄清石灰水:
③往氯化铝溶液中加入足量的NaOH溶液:
(Ⅲ)写出下列反应的化学方程式:
①二氧化硫发生催化氧化反应:
②氯气与氢氧化钠溶液反应:
③铜片与稀硝酸的反应:
 Fe3O4+4H2
Fe3O4+4H2 2H2↑+ O2↑
2H2↑+ O2↑ | A.分子中的原子重新组合 | B.氧元素的得失 |
| C.电子的得失或共用电子对的偏移 | D.化合价的改变 |
(每空2分,共16分)短周期元素X、Y、Z、W,原子序数依次增大。常温常压下,只有W的单质为气体。它们的最高氧化物对应的水化物依次为甲、乙、丙、丁。甲、乙、丙是中学化学中的常见物质,其中只有乙难溶于水,且能和甲、丙反应得到澄清溶液。根据以上信息填写下列空白:
⑴画出W的原子结构示意图_________________________________________;
⑵将乙和甲、丙分别反应后得到的溶液混合,观察到的现象是___________________
___________________ ,两溶液混合时所发生反应的离子方程式为____________________________________________________;
⑶下列事实能证明Z和W非金属性强弱的是(选填序号)__________________________;
| A.单质的熔点:Z>W2 |
| B.酸性:丁>丙 |
| C.在溶液中:W2+H2Z=2HW+Z |
| D.稳定性:HW>H2Z |
(每空2分,共18分)Ⅰ.已知: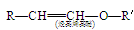
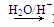 R—CH2CHO+R′OH烃基烯基醚A的相对分子质量(Mr)为176,分子中碳氢原子数目比为3∶4。与A相关的反应如下:
R—CH2CHO+R′OH烃基烯基醚A的相对分子质量(Mr)为176,分子中碳氢原子数目比为3∶4。与A相关的反应如下: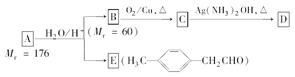
请回答下列问题:
(1)A的分子式为________。
(2)B的名称是________;
(3)写出C―→D反应的化学方程式:
________________________________________________________________________。
(4)写出两种同时符合下列条件的E的同分异构体的结构简式:________、________。
①属于芳香醛;
②苯环上有两种不同环境的氢原子。
Ⅱ.由E转化为对甲基苯乙炔
(5)写出①~④步反应所加试剂、反应条件和①~③步反应类型:
| 序号 | 所加试剂及反应条件 | 反应类型 |
| ① | | |
| ② | | |
| ③ | | |
| ④ | | |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com