
题目列表(包括答案和解析)
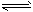 2C(g)+xD(s)的化学平衡状态。相关数据如下:M中初始加入3mol A、2mol B,2min后达到平衡时生成1. 2mol D,测得从反应开始到平衡,C的速率为 0. 3mol/(L·min)。N中初始加入2molC、
2C(g)+xD(s)的化学平衡状态。相关数据如下:M中初始加入3mol A、2mol B,2min后达到平衡时生成1. 2mol D,测得从反应开始到平衡,C的速率为 0. 3mol/(L·min)。N中初始加入2molC、| A、x=1 | B、平衡时B与C的浓度之比为3:2 | C、A与B的转化率相等,均为40% | D、由体系中混合气体的密度不变,不能判断该反应已达到平衡状态 |
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
恒温下,容积均为2L的密闭容器M、N中,分别有以下两种起始投料建立的可逆反应:
3A(g)+2B(g)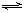 2C(g)+xD(s)的化学平衡状态,相关数据如下:M:3molA、2molB,2min达到平衡时,生成D1.2mol,测得从反应开始到平衡时C的反应速率为0.3mol/(L?min)。N:2molC、ymolD;达平衡时c(A)=0.6mol?L-1。下列推断的结论中不正确的是 ()。
2C(g)+xD(s)的化学平衡状态,相关数据如下:M:3molA、2molB,2min达到平衡时,生成D1.2mol,测得从反应开始到平衡时C的反应速率为0.3mol/(L?min)。N:2molC、ymolD;达平衡时c(A)=0.6mol?L-1。下列推断的结论中不正确的是 ()。
A.x=2 B.平衡时M中c(A)<0.6mol/L
C.y>0.8 D.y<0.8
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com