
题目列表(包括答案和解析)
(14分)已知:化合物B、C、E中含有两种相同的元素,A可用于玻璃、洗涤剂等的生产,B可用于制作光纤,G的组成元素与D相同。这些化合物之间存在下图所示的转化关系。
请回答:
(1)在化合物A、C、F中含有的相同元素 。
(2)化合物C的化学式为 ,其水溶液的pH 7(填“>”或“<”)。
(3) 700 ℃时,向容积为2 L的密闭容器中充入一定量的G(g)和H2O(g),发生反应:
G(g)+H2O(g) D(g)+H2(g)。反应过程中测定的部分数据见下表(表中t1>t2):
| 反应时间/min | n(G)/mol | n(H2O)/ mol |
| 0 | 1.20 | 0.60 |
| t1 | 0.80 |
|
| t2 |
| 0.20 |
① 反应在t1min内的平均速率为v(H2)= mol/(L·min)
② 保持其他条件不变,起始时向容器中充入0.60 mol G和1.20 mol H2O,到达平衡时,
n(D)= mol。
③ 温度升至800℃,上述反应平衡常数为0.64,则正反应为 反应(填“放热”或“吸热”)。
(14分)已知:化合物B、C、E中含有两种相同的元素,A可用于玻璃、洗涤剂等的生产,B可用于制作光纤,G的组成元素与D相同。这些化合物之间存在下图所示的转化关系。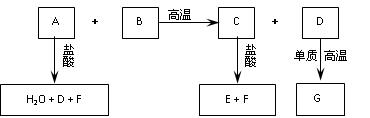
请回答:
(1)在化合物A、C、F中含有的 相同元素 。
相同元素 。
(2)化合物C的化学式为 ,其水溶液的pH 7(填“>”或“<”) 。
。
(3) 700 ℃时,向容积为 2 L的密闭容器中充入一定量的G(g)和H2O(g),发生反应:
2 L的密闭容器中充入一定量的G(g)和H2O(g),发生反应:
G(g)+H2O(g)  D(g)+H2(g)。反应过程中测定的部分数据见下表(表中t1>t2):
D(g)+H2(g)。反应过程中测定的部分数据见下表(表中t1>t2):
| 反应时间/min | n(G)/mol | n(H2O)/ mol |
| 0 | 1.20 | 0.60 |
| t1 | 0.80 | |
| t2 | | 0.20 |
(14分)已知:化合物B、C、E中含有两种相同的元素,A可用于玻璃、洗涤剂等的生产,B可用于制作光纤,G的组成元素与D相同。这些化合物之间存在下图所示的转化关系。
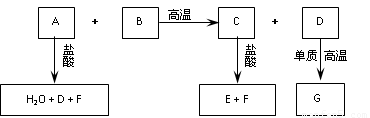
请回答:
(1)在化合物A、C、F中含有的相同元素 。
(2)化合物C的化学式为 ,其水溶液的pH 7(填“>”或“<”)。
(3) 700 ℃时,向容积为2 L的密闭容器中充入一定量的G(g)和H2O(g),发生反应:
G(g)+H2O(g)  D(g)+H2(g)。反应过程中测定的部分数据见下表(表中t1>t2):
D(g)+H2(g)。反应过程中测定的部分数据见下表(表中t1>t2):
|
反应时间/min |
n(G)/mol |
n(H2O)/ mol |
|
0 |
1.20 |
0.60 |
|
t1 |
0.80 |
|
|
t2 |
|
0.20 |
① 反应在t1min内的平均速率为v(H2)= mol/(L·min)
② 保持其他条件不变,起始时向容器中充入0.60 mol G和1.20 mol H2O,到达平衡时,
n(D)= mol。
③ 温度升至800℃,上述反应平衡常数为0.64,则正反应为 反应(填“放热”或“吸热”)。
工业上一般在恒容密闭容器中可以采用下列反应合成甲醇:
CO(g) + 2H2(g) ![]() CH3OH(g) Δ H
CH3OH(g) Δ H
(1)判断反应达到平衡状态的依据是 (填序号)。
a. 生成CH3OH的速率与消耗CO的速率相等
b. 混合气体的密度不变 c. 混合气体的相对平均分子质量不变
d. CH3OH、CO、H2的浓度都不再发生变化
(2)下表所列数据是反应在不同温度下的化学平衡常数(K)。
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
①由表中数据判断ΔH 0 (填“>”、“=”或“<”)。
②要提高CO的转化率,可以采取的措施是_________(填序号)。
a.升温 b.加入催化剂 c.增加CO的浓度
d.加入H2加压 e.加入惰性气体加压 f.分离出甲醇
③某温度下,将2 mol CO和6 mol H2充入2 L的密闭容器中,充分反应10min后,达到平衡时测得c(CO)= 0.2 mol/L,则CO的转化率为 ,此时的温度为 。以CH3OH表示该过程的反应速率
v(CH3OH)= mol /(L · min)。
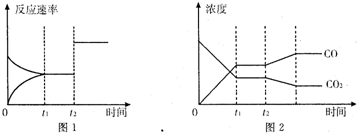
(3)图一表示在温度分别为T1、T2时,平衡体系中H2的体积分数随压强变化曲线,A、C两点的反应速率A____C(填“>”、“=”或“<”,下同),A、C两点的化学平衡常数A_____C,由状态B到状态A,可采用______的方法(填“升温”或“降温”)。


(4)一定条件下,0.5mol甲醇蒸气完全燃烧生成二氧化碳气体和液态水,放出QKJ的热量。写出该反应的热化学方程式 。
图二是甲醇燃料电池(电解质溶液为KOH溶液)结构示意图,写出 a处电极上发生的电极反应式 。
| 温度/ | 400 | 500 | 800 |
| 平衡常数Kc | 9.94 | 9 | 1 |
| 时间(min) | CO(g) | H2O(g) | CO2(g) | H2(g) |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.120 | 0.220 | 0.080 | 0.080 |
| 3 | 0.080 | 0.180 | 0.120 | 0.120 |
| 4 | 0.100 | 0.200 | 0.100 | C1 |
| 5 | 0.067 | 0.267 | 0.133 | C2 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com